题目内容
室温时,将浓度和体积分别为c1、V1的盐酸溶液和c2、V2的氨水溶液相混合,下列关于该混合溶液的叙述错误的是( )
| A、若pH<7时,则一定是c1V1=c2V2 |
| B、该混合液中,c(NH4+)+c(H+)═c(Cl-)+c(OH-) |
| C、当pH=7时,若V1=V2,则一定是c2> c1 |
| D、若V1=V2,c1=c2,则c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:A、当溶液呈酸性时,溶液中氢离子浓度小于氢氧根离子浓度,但混合时氯化氢与一水合氨的物质的量不一定相等;
B、溶液中一定满足电荷守恒,根据混合液中的电荷守恒进行判断;
C、氯化铵为强酸弱碱盐,其水溶液呈酸性,若要使其呈中性,氨水应该稍过量;
D、当氯化氢和一水合氨的物质的量相等时,根据电荷守恒判断溶液中各离子浓度的关系.
B、溶液中一定满足电荷守恒,根据混合液中的电荷守恒进行判断;
C、氯化铵为强酸弱碱盐,其水溶液呈酸性,若要使其呈中性,氨水应该稍过量;
D、当氯化氢和一水合氨的物质的量相等时,根据电荷守恒判断溶液中各离子浓度的关系.
解答:
解:A、氨水是弱碱,盐酸为强酸,所以等物质的量的酸和碱混合时,溶液呈酸性,当盐酸过量时溶液也呈酸性,所以当pH<7时,一定是c1v1≥c2v2,故A错误;
B、根据混合液中的电荷守恒可知,c(NH4+)+c(H+)═c(Cl-)+c(OH-),故B正确;
C、氯化铵为强酸弱碱盐,其水溶液呈酸性,若要使混合溶液呈中性,氨水应该稍过量,所以当pH=7时,若v1=v2,则一定是c2>c1,故C正确;
D、如果V1=V2,c1=c2,则氯化氢和一水合氨的物质的量相等,混合后恰好反应生成氯化铵,溶液显示酸性,则c(H+)>c(OH-),根据电荷守恒c(NH4+)+c(H+)═c(Cl-)+c(OH-)可得:c(Cl-)>c(NH4+),则溶液中离子浓度大小为:c(Cl-)>c(NH4+)>c(H+)>c(OH-),故D正确;
故选A.
B、根据混合液中的电荷守恒可知,c(NH4+)+c(H+)═c(Cl-)+c(OH-),故B正确;
C、氯化铵为强酸弱碱盐,其水溶液呈酸性,若要使混合溶液呈中性,氨水应该稍过量,所以当pH=7时,若v1=v2,则一定是c2>c1,故C正确;
D、如果V1=V2,c1=c2,则氯化氢和一水合氨的物质的量相等,混合后恰好反应生成氯化铵,溶液显示酸性,则c(H+)>c(OH-),根据电荷守恒c(NH4+)+c(H+)═c(Cl-)+c(OH-)可得:c(Cl-)>c(NH4+),则溶液中离子浓度大小为:c(Cl-)>c(NH4+)>c(H+)>c(OH-),故D正确;
故选A.
点评:本题考查了酸碱混合溶液的定性判断、溶液中离子浓度大小比较,题目难度中等,注意掌握溶液酸碱性的定性判断方法,根据溶液中物料守恒和电荷守恒即可解答本题,该知识点是学习的难点,也是考试的热点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰.在纸内的离子“流过”水和氧化锌组成的电解液.电池总反应为:Zn+2MnO2+H2O═ZnO+2MnO(OH).下列说法正确的是( )
| A、该电池的正极为锌 |
| B、该电池反应中二氧化锰起催化剂作用 |
| C、电池负极反应式为:Zn+2OH--2e-═ZnO+H2O |
| D、当 0.l mol Zn 完全溶解时,流经电解液的电子个数为1.204×l023 |
在一个V升的密闭容器中放入2L A气体和1L B气体,在一定条件下发生反应:3A(g)+B(g)?nC(g)+2D(g),达到平衡后,A的浓度减小,混合气体的平均分子量增大,则该反应方程式中n值是( )
| A、1 | B、2 | C、3 | D、4 |
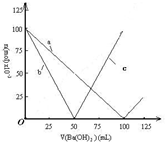 烧杯中盛有100mL 0.1mol/L的NaHSO4溶液,向其中逐滴滴加0.1mol/L的Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图.下列说法正确的是( )
烧杯中盛有100mL 0.1mol/L的NaHSO4溶液,向其中逐滴滴加0.1mol/L的Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图.下列说法正确的是( )| A、曲线a表示Ba2+的物质的量的变化 |
| B、曲线c表示OH-的物质的量的变化 |
| C、加入Ba(OH)2溶液50mL反应的离子方程式为Ba2++OH-+H++SO42-→BaSO4↓+H2O |
| D、加入Ba(OH)2溶液大于50mL后,反应的离子方程式为 OH-+H+→H2O |
已知:H2(g)+
O2(g)=H2O(g)△H=-242kJ/mol,断开1 mol O=O键和1 molH-O键所吸收的能量分别为496 kJ和463kJ,则断开1 mol H-H键所吸收的能量为( )
| 1 |
| 2 |
| A、920 kJ |
| B、557 kJ |
| C、436 kJ |
| D、188 kJ |
25℃、101kPa 下:①2Na(s)+
O2(g)→Na2O(s)+414KJ②2Na(s)+O2(g)→Na2O2(s)+511KJ
下列说法正确的是( )
| 1 |
| 2 |
下列说法正确的是( )
| A、①和②产物的阴阳离子个数比不相等 |
| B、①和②生成等物质的量的产物,转移电子数相同 |
| C、Na2O2(s)比Na2O(s)稳定 |
| D、1 mol Na2O2(s)与1 mol Na2O(s)所含的能量相差97kJ |
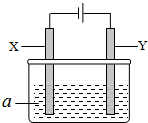 电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: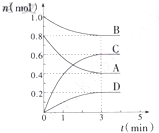 在T℃时,在容积为0.5L的密闭容器中发生如下反应:mA(g)+nB(g)?pC(g)+qD(s),△H<0(m、n、p、q为最简整数比).A、B、C、D物质的量的变化如图所示:
在T℃时,在容积为0.5L的密闭容器中发生如下反应:mA(g)+nB(g)?pC(g)+qD(s),△H<0(m、n、p、q为最简整数比).A、B、C、D物质的量的变化如图所示: