题目内容
16.下列有关氯元素单质及其化合物性质的说法正确的是.| A. | 液氯是纯净物,氯水是电解质,漂白粉是混合物 | |
| B. | 氯气可用作消毒剂和漂白剂,是因为氯分子具有强氧化性 | |
| C. | 随着化合价的升高,氯的含氧酸酸性和氧化性均逐渐增强 | |
| D. | 不能用pH试纸测定氯水的pH |
分析 A.氯水为混合物,而电解质必须为化合物;
B.干燥的氯气不具有漂白性;
B.随着化合价的升高,氯的含氧酸酸性增强,氧化性逐渐减弱;
D.氯水中HClO具有漂白性.
解答 解:A.氯水为混合物,而电解质必须为化合物,则氯气不是电解质,而液氯是纯净物,漂白粉(主要成分为氯化钙和次氯酸钙)是混合物,故A错误;
B.干燥的氯气不具有漂白性,氯气具有强氧化性,氯气可用作消毒剂,故B错误;
B.随着化合价的升高,非羟基氧原子个数增多,则氯的含氧酸酸性增强,而氧化性逐渐减弱,故C错误;
D.氯水中HClO具有漂白性,则不能用pH试纸测定氯水的pH,故D正确;
故选D.
点评 本题考查含氯物质的性质,为高频考点,把握氯气的性质、性质与用途等为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
6.在碱性条件下,1mol某饱和羧酸酯完全水解可得到1mol甘油和3mol羧酸钠,且羧酸钠酸化后的产物与戊醇的相对分子质量相等,则该饱和羧酸酯的分子式为( )
| A. | C12H20O6 | B. | C15H26O6 | C. | C18H32O6 | D. | C21H38O6 |
4.下列微粒中:①12Mg2+ ②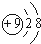 ③NH4+ ④O2-,核外电子总数相同的是( )
③NH4+ ④O2-,核外电子总数相同的是( )
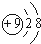 ③NH4+ ④O2-,核外电子总数相同的是( )
③NH4+ ④O2-,核外电子总数相同的是( )| A. | ②③④ | B. | ①②③④ | C. | ①②③ | D. | ①③④ |
1.为鉴别卤代烃中所含卤素原子,现有下列实验操作步骤,正确的顺序是( )
①加入AgNO3溶液 ②加入少许卤代烃试样 ③加热 ④加入5mL 4mol•L-1 NaOH溶液 ⑤加入5mL 4mol•L-1 HNO3溶液.
①加入AgNO3溶液 ②加入少许卤代烃试样 ③加热 ④加入5mL 4mol•L-1 NaOH溶液 ⑤加入5mL 4mol•L-1 HNO3溶液.
| A. | ②④③①⑤ | B. | ②③①④⑤ | C. | ②④③⑤① | D. | ②⑤③①④ |
8.下列递变规律不正确的是( )
| A. | Na.Mg、Al还原性依次减弱 | B. | I2、Br2、Cl2氧化性依次增强 | ||
| C. | 原子半径:F<Mg<K | D. | 稳定性:PH3>H2S>HCl |
10.在通常条件下,下列各组物质的性质排列正确的是( )
| A. | Na、Mg、Al的第一电离能逐渐增大 | B. | 热稳定性:HF>H2O>NH3 | ||
| C. | S2-、Cl-、K+的半径逐渐增大 | D. | O、F、Ne的电负性逐渐增大 |