题目内容
下列是元素周期表的前三周期中的部分元素:
(1)①~⑨这些元素中,最活泼的金属元素是 ,最不活泼的非金属元素是 .(填写元素符号)
(2)写出⑧的原子结构示意图 .
(3)写出⑥的最高价氧化物和④的最高价氧化物对应的水化物反应的化学方程式 .
(4)①、②、③的氢化物的稳定性由强到弱的顺序是: (用化学式表示)

(1)①~⑨这些元素中,最活泼的金属元素是
(2)写出⑧的原子结构示意图
(3)写出⑥的最高价氧化物和④的最高价氧化物对应的水化物反应的化学方程式
(4)①、②、③的氢化物的稳定性由强到弱的顺序是:
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由①~⑨这些元素在元素周期表内的相对位置可知,①到⑨分别是N、O、F、Na、Mg、Al、S、Cl、Ar,然后回答上述问题.
解答:
解:(1)①~⑨这些元素中,最活泼的金属元素在周期表的左下角,为Na元素,不活泼的非金属元素稀有气体Ar,故答案为:Na;Ar;
(2)⑧是氯元素,其原子结构示意图 ,故答案为:
,故答案为: ;
;
(3)⑥的最高价氧化物是Al2O3和④的最高价氧化物对应的水化物是NaOH,两者反应的化学方程式为Al2O3+2NaOH=2NaAlO2+H2O,
故答案为:Al2O3+2NaOH=2NaAlO2+H2O;
(4)①、②、③的氢化物的稳定性由强到弱的顺序与非金属强弱一致,即HF>H2O>NH3,故答案为:HF>H2O>NH3.
(2)⑧是氯元素,其原子结构示意图
 ,故答案为:
,故答案为: ;
;(3)⑥的最高价氧化物是Al2O3和④的最高价氧化物对应的水化物是NaOH,两者反应的化学方程式为Al2O3+2NaOH=2NaAlO2+H2O,
故答案为:Al2O3+2NaOH=2NaAlO2+H2O;
(4)①、②、③的氢化物的稳定性由强到弱的顺序与非金属强弱一致,即HF>H2O>NH3,故答案为:HF>H2O>NH3.
点评:本题考查元素化合物的性质,难度不大,学生只要认真审题,按要求回答即可!

练习册系列答案
相关题目
某同学对一无色透明溶液进行分析得出该溶液中含有下列某组离子,你认为该组离子应该是( )
| A、Al3+、NO3-、K+、SO42- |
| B、Ca2+、H+、HCO3-、Na+ |
| C、OH-、CO32-、Cu2+、SO42- |
| D、Fe3+、Mg2+、NO3-、Cl- |
下列金属或氧化物可以完全溶解的是( )
| A、1mol Zn与含1mol HCl的稀盐酸共热 |
| B、1mol Cu与含2mol H2SO4的浓硫酸共热 |
| C、1mol Cu与含4mol HNO3的浓硝酸 |
| D、1mol MnO2与含4mol HCl的浓盐酸共热 |
某高分子化合物的结构简式为 ,该物质可由下列哪组物质为原料直接合成得到( )
,该物质可由下列哪组物质为原料直接合成得到( )
 ,该物质可由下列哪组物质为原料直接合成得到( )
,该物质可由下列哪组物质为原料直接合成得到( )A、 和CH3CH2OH 和CH3CH2OH |
B、 和HOCH2CH2OH 和HOCH2CH2OH |
C、 和CH3CH2OH 和CH3CH2OH |
D、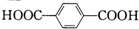 和HOCH2CH2OH 和HOCH2CH2OH |


