题目内容
6.下列说法正确的是( )| A. | 反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的△H<0 | |
| B. | △H<0、△S<0的反应在高温条件下能自发进行 | |
| C. | 反应CaCO3(s)=CaO(s)+CO2(g)的△S<0 | |
| D. | 同一物质的固、液、气三种状态的熵值相同 |
分析 A.由反应可知△S<0,△H-T△S<0的反应可自发进行;
B.△H-T△S<0的反应可自发进行;
C.该反应中气体增加;
D.混乱度越大,熵越大.
解答 解:A.由反应可知△S<0,能自发进行,由△H-T△S<0的反应可自发进行,则该反应的△H<0,故A正确;
B.△H-T△S<0的反应可自发进行,可知△H<0、△S<0的反应在低温条件下能自发进行,故B错误;
C.该反应中气体增加,则△S>0,故C错误;
D.混乱度越大,熵越大,则同一物质的固、液、气三种状态的熵值由小到大,故D错误;
故选A.
点评 本题考查反应热与焓变,为高频考点,把握反应进行方向的判断、混乱度的判断为解答的关键,侧重分析与应用能力的考查,注意选项B为易错点,题目难度不大.

练习册系列答案
相关题目
17.关于下列各装置图的叙述中,正确的是( )
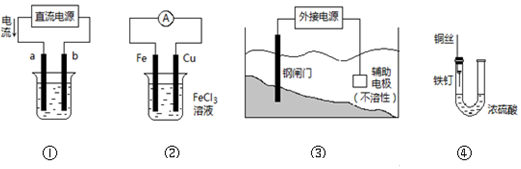

| A. | 用装置①精炼铜,则b为粗铜,电解质溶液为CuSO4溶液 | |
| B. | 装置②的总反应是:Cu+2Fe3+═Cu2++2Fe2+ | |
| C. | 装置③中钢闸门应与外接电源的负极相连被保护,该方法叫做牺牲阳极的阴极保护法 | |
| D. | 装置④中的铁钉不容易被腐蚀 |
14.相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)?2NH3(g)△H=-92.6kJ•mol-1.
实验测得起始、平衡时的有关数据如表所示:
下列叙述错误的是( )
N2(g)+3H2(g)?2NH3(g)△H=-92.6kJ•mol-1.
实验测得起始、平衡时的有关数据如表所示:
| 容器 编号 | 起始时各物质的物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15 kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
| A. | 容器①、②中反应的平衡常数相等 | |
| B. | 平衡时,两个容器中NH3的体积分数相等 | |
| C. | 若容器①的体积为0.5 L,则平衡时放出的热量小于23.15 kJ | |
| D. | 容器②中达平衡时放出的热量Q=23.15 kJ |
1.下列现象不涉及胶体性质的是( )
| A. | 放电影时,放映室射到银幕上的光柱 | |
| B. | 肾衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 | |
| C. | 在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀 | |
| D. | 加电解质可使某种胶体聚沉,这是中和胶体粒子所带电荷的缘故 |
11.现有H2S、NH3、CH4三种气体,它们分别都含有相同数目的氢原子,则三种气体的物质的量之比为( )
| A. | 1:1:1 | B. | 2:3:4 | C. | 6:4:3 | D. | 6:3:4 |
18.类推是化学学习和研究中常用的思维方法.下列类推正确的是( )
| A. | Mg和Al较活泼,必须通过电解熔融MgCl2和AlCl3制取 | |
| B. | 金属Ma着火不能用干冰灭火,金属Na着火也不能用干冰灭火 | |
| C. | SO2能使品红溶液褪色,CO2也能使品红溶液褪色 | |
| D. | F2、Cl2、Br2、I2的熔点依次升高,N2、P4、As、Sb、Bi的熔点也依次升高 |
15.利用实验器材(规格和数量不限)能完成相应实验的一项是( )
| 选项 | 实验器材(省略夹持装置) | 相应实验 |
| A | 烧杯、玻璃棒、蒸发皿 | CuSO4溶液的浓缩结晶 |
| B | 烧杯、玻璃棒、胶头滴管、滤纸 | 用盐酸除去BaSO4中少量的BaCO3 |
| C | 烧杯、玻璃棒、胶头滴管、容量瓶 | 用固体NaCl配制0.5mol/L的溶液 |
| D | 烧杯、玻璃棒、胶头滴管、分液漏斗 | 用溴水和CCl4除去NaBr溶液中少量的NaI |
| A. | A | B. | B | C. | C | D. | D |
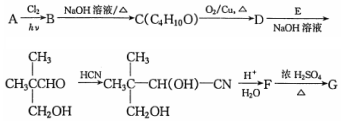
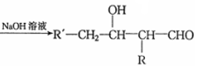
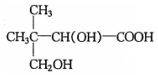 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$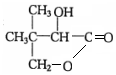 +H2O.F能发生缩聚反应,则生成链节的主链上有四个碳愿子的高分子化合物的结构简式为
+H2O.F能发生缩聚反应,则生成链节的主链上有四个碳愿子的高分子化合物的结构简式为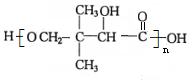 .
.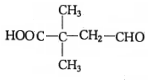 .
.