题目内容
【题目】化学平衡常数(K)、电离常数(Ka、Kb)、水的离子积常数(Kw)、溶度积常数(Ksp)等常数是表示判断物质性质的重要常数,下列关于这些常数的说法中,正确的是![]()
A.化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关
B.Ka(HCN)<Ka(CH3COOH)说明相同物质的量浓度时,氢氰酸的酸性比醋酸的强
C.当温度升高时,弱酸、弱碱的电离常数(Ka、Kb)和水的离子积常数(Kw)均变大
D.向氯化钡溶液中加入等体积同浓度的碳酸钠和硫酸钠溶液,先产生![]() 沉淀,则Ksp(BaSO4)>Ksp(BaCO3)
沉淀,则Ksp(BaSO4)>Ksp(BaCO3)
【答案】C
【解析】
本题考查各类平衡常数的应用,运用各类平衡常数的概念和平衡常数只与温度有关分析。
![]() 化学平衡常数只与温度有关,与浓度、压强、催化剂无关,故A错误;
化学平衡常数只与温度有关,与浓度、压强、催化剂无关,故A错误;
B.二者都是一元酸,浓度相同时,电离常数越小,说明电离程度越小,氢离子浓度越小,溶液的酸性越弱,故等物质的量浓度的氢氰酸的酸性比醋酸弱,故B错误;
C.弱酸、弱碱和水的电离过程是吸热过程,温度升高促进电离,弱酸、弱碱和水的离子积的电离常数(Ka、Kb、Kw)变大,故C正确;
D.溶解度越小越先沉淀,二者结构相似,溶解度越小,溶度积就越小,故Ksp(BaSO4)<Ksp(BaCO3),故D错误;
答案选C。

【题目】核安全与放射性污染防治已引起广泛关注。在爆炸的核电站周围含有放射性物质 碘-131和钙-137。碘-131 —旦被人体吸入,可能会引发甲状腺肿大等疾病。
(1)与钠同主族的前四周期(包括第四周期)的三种元素X、Y、Z的第一电离能如下表:
元素代号 | X | Y | Z |
第一电离能/(kJ.mol) | 520 | 496 | 419 |
基态Z原子倒数第二层电子的排布式为______。X、Y、Z三种元素形成的单质熔点由高到低的顺序为_______(用元素符号表示),其原因为___________ .
(2)F与I同主族,BeF2分子中心原子的杂化类型为_________ ,BeF2分子是________分子(选填“极性”或“非极性”)。
(3)已知高碘酸有两种形式,化学式分别为H5IO6  和HIO4 ,二者酸性强弱顺序为:H5IO6 ________HIO4(选填">"或"<"“=”)。从电子云的重叠方式的角度分析,H5IO6分子中的化学键有________(写出两种).
和HIO4 ,二者酸性强弱顺序为:H5IO6 ________HIO4(选填">"或"<"“=”)。从电子云的重叠方式的角度分析,H5IO6分子中的化学键有________(写出两种).
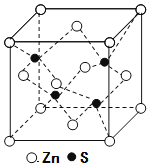
(4)131I2晶体的晶胞结构如图甲所示,该晶胞中平均含有________个131I原子,晶体中碘分子的排列有_________种不同的方向。

(5)KI的晶胞结构如图乙所示,每个K+周围紧邻的K+个数为_______个。KI晶体的密度为ρg.cm-3 ,K和I的原子半径分别为rkcm和rI cm,阿伏加德罗常数的值为NA,则 KI晶胞中的空间利用率为_______. [空间利用率=(球体积/晶胞体积)×100%,用相关字母的代数式表示即可]