题目内容
13.水溶液中下列电离方程式书写正确的是( )| A. | Ca(OH)2?Ca2++2OH- | B. | NaHCO3═Na++H++CO32- | ||
| C. | H2SO3?2H++SO32- | D. | BaSO4═Ba2++SO42- |
分析 A.氢氧化钙为强电解质,完全电离用等号;
B.碳酸氢钠为强电解质,电离生成钠离子和碳酸氢根离子;
C.亚硫酸为二元弱酸,分步电离,以第一步为主;
D.硫酸钡为强电解质,完全 电离.
解答 解:A.氢氧化钙为强电解质,完全电离,电离方程式:Ca(OH)2=Ca2++2OH-,故A错误;
B.碳酸氢钠为强电解质,电离生成钠离子和碳酸氢根离子,电离方程式:NaHCO3═Na++HCO3-,故B错误;
C.亚硫酸为二元弱酸,分步电离,以第一步为主,电离方程式:H2SO3?H++HSO3-,故C错误;
D.硫酸钡为强电解质,完全 电离,电离方程式:BaSO4═Ba2++SO42-,故D正确;
故选:D.
点评 本题考查了电解质电离方程式的书写,明确电解质强弱及电离方式是解题关键,注意电离方程式遵循客观事实、遵循电荷守恒规律,遵循原子个数守恒规律.

练习册系列答案
相关题目
5.要想证明某溶液中是否含有Fe3+,下列操作中正确的是( )
| A. | 通入氯气 | B. | 加入硝酸 | C. | KSCN溶液 | D. | 加入硫酸 |
4.将一定质量金属M的粉末放入盛有硝酸铜溶液的烧杯中,充分反应后溶液呈无色;继续向烧杯中加入一定量的硝酸银溶液,待充分反应后过滤,得蓝色滤液和滤渣.根据实验分析,以下结论错误的是( )
| A. | 金属活动性顺序:M>Cu>Ag | |
| B. | 滤液中一定含有M的阳离子和Cu2+ | |
| C. | 滤渣中一定含有Ag和Cu | |
| D. | 向滤液中滴加稀盐酸,可能产生白色沉淀 |
1.分析如图所示装置,下列叙述不正确的是( )


| A. | 左边装置是氢氧燃料电池,右边装置是电镀池 | |
| B. | 电子流动方向:b→Zn→CuSO4(aq)→Cu→a | |
| C. | 一段时间后,左端溶液浓度变小,右端溶液浓度不变 | |
| D. | 左边装置中的电池反应为:2H2+O2=2H2O |
16.下列有机物的命名正确的是( )
| A. | CH3CH2CH(CH3)CH(CH3)OH:3-甲基-2-戊醇 | |
| B. | CH3CH(CH3)CH═CH2:3-甲基丁烯 | |
| C. | CH3CH2C(CH3)2CH3:2,2-甲基丁烷 | |
| D. | CH2Cl-CH2Cl:二氯乙烷 |
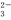 、SO
、SO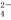 ,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液。检验其中OH-的实验方法省略,检验其他阴离子的过程如下图所示。
,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液。检验其中OH-的实验方法省略,检验其他阴离子的过程如下图所示。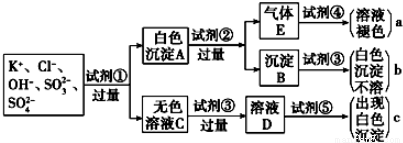
 是_____________________。
是_____________________。
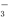 的物质的量浓度为( )
的物质的量浓度为( )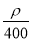 mol·L-1 B.
mol·L-1 B.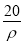 mol·L-1 C.
mol·L-1 C.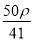 mol·L-1 D.
mol·L-1 D. mol·L-1
mol·L-1