题目内容
16.氯气之所以长期用于自来水消毒,原因是( )| A. | 氯气有毒,可以毒死细菌、病毒 | |
| B. | 氯气具有刺激性气味,可以熏死细菌、病毒 | |
| C. | 氯气与水反应生成具有强氧化性的HClO,可以杀死细菌、病毒 | |
| D. | 氯气是绿色气体,不会污染空气 |
分析 氯气与水反应生成具有强氯化性的HClO,可以杀死细菌、病毒,以此来解答.
解答 解:氯气用于自来水消毒的原因是氯气与水反应生成具有强氯化性的HClO,可以杀死细菌、病毒,则氯气长期用于自来水消毒,
而与气味、毒性无关,其中氯气有毒,会污染空气,
故选C.
点评 本题考查氯气的化学性质,为高频考点,把握氯气与水的反应及HClO的性质为解答的关键,注重化学与生活的联系,题目难度不大.

练习册系列答案
相关题目
7.浓硝酸不具有的性质是( )
| A. | 不稳定性 | B. | 可溶解水晶 | C. | 强氧化性 | D. | 易挥发性 |
1.下列叙述中正确的是( )
| A. | 相同条件下,N2和O3的混合气体与等体积的N2所含原子数相等 | |
| B. | 标准状况下,28 g CO和22.4 L H2O所含分子数相等 | |
| C. | 5.6 g铁粉与足量盐酸充分反应,有0.2 mol电子转移 | |
| D. | 等质量的CH4和NH3所含电子数相等 |
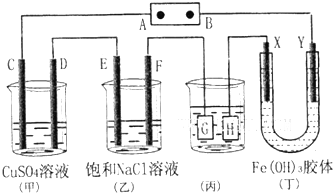
8.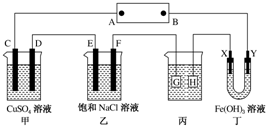 如图所示的装置,C、D、E、F、X、Y都是惰性电极.将电池接通后,向乙中滴入酚酞溶液,在F极附近溶液显红色.则以下说法正确的是( )
如图所示的装置,C、D、E、F、X、Y都是惰性电极.将电池接通后,向乙中滴入酚酞溶液,在F极附近溶液显红色.则以下说法正确的是( )
 如图所示的装置,C、D、E、F、X、Y都是惰性电极.将电池接通后,向乙中滴入酚酞溶液,在F极附近溶液显红色.则以下说法正确的是( )
如图所示的装置,C、D、E、F、X、Y都是惰性电极.将电池接通后,向乙中滴入酚酞溶液,在F极附近溶液显红色.则以下说法正确的是( )| A. | 电源B极是正极 | |
| B. | 甲、乙装置的C、D、E、F电极均有单质生成,其物质的量之比为1:2:2:1 | |
| C. | 欲用丙装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液 | |
| D. | 装置丁中Y极附近红褐色变深,说明氢氧化铁胶粒带正电荷 |
5.以下几个热化学方程式,能表示燃烧热的热化学方程式是( )
| A. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=110.5 kJ•mol-1 | |
| B. | C(s)+O2(g)═CO2(g)△H=-393.5 kJ•mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1 | |
| D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8 kJ•mol-1 |
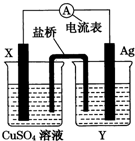 依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池,如图所示.请回答下列问题.
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池,如图所示.请回答下列问题.