题目内容
7.浓硝酸不具有的性质是( )| A. | 不稳定性 | B. | 可溶解水晶 | C. | 强氧化性 | D. | 易挥发性 |
分析 硝酸属于酸,具有酸的通性,硝酸还具有强氧化性、不稳定性、挥发性,据此分析解答.
解答 解:A.浓硝酸能分解生成二氧化氮、氧气和水,所以浓硝酸不稳定,要避光保存,故A错误;
B.二氧化硅是酸性氧化物,不与硝酸反应,故B正确;
C.浓硝酸中N元素处于最高价态,处于最高价态是元素具有强氧化性,能氧化部分较不活泼的金属,故C错误;
D.浓硝酸、浓盐酸都具有挥发性,所以要密封保存,故D错误;
故选B.
点评 本题考查了浓硝酸的性质,知道浓硝酸具有“酸性、强氧化性、挥发性、不稳定性”等,且硝酸的强氧化性与其浓度有关,浓度导致浓硝酸、稀硝酸的强氧化性不同,浓硝酸和铁、铝在常温下易发生钝化现象.

练习册系列答案
相关题目
17.根据图所示的信息,判断下列叙述不正确的是( )
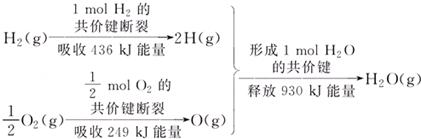

| A. | 1 mol H2的共价键形成放出436 kJ能量 | |
| B. | 氢气跟氧气反应生成水的同时吸收能量 | |
| C. | 1 mol H2(g)跟0.5mol O2(g)反应生成1 mol H2O(g)释放能量245 KJ | |
| D. | 1 mol H2(g)与0.5mol O2(g)的总能量大于1 mol H2O(g)的能量 |
2.乙硼烷(B2H6)是一种潜在的高能燃料,工业上可用反应:B2O3+2Al+3H2$\frac{\underline{\;AlCl_{3}\;}}{高压}$Al2O3+B2H6制取,下列有关说法正确的是( )
| A. | 反应中氢气作还原剂,铝作氧化剂 | B. | B2H6充分燃烧生成B2O3和H2O | ||
| C. | B2H6中存在共价键和离子键 | D. | 每生成1molB2H6转移3mol电子 |
12.下列物质间的反应不属于离子反应的是( )
| A. | CO+O2 | B. | NaCl+AgNO3 | C. | CaCO3+HCl | D. | CuO+H2 |
19.下列说法正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 天然气、太阳能、生物质能、风能、氢能均属于新能源 | |
| C. | 自发反应的熵一定增大,非自发反应的熵一定减小 | |
| D. | 常温下,反应C(s)+CO2(g)?2CO(g)不能自发进行,则该反应的△H>0 |
16.氯气之所以长期用于自来水消毒,原因是( )
| A. | 氯气有毒,可以毒死细菌、病毒 | |
| B. | 氯气具有刺激性气味,可以熏死细菌、病毒 | |
| C. | 氯气与水反应生成具有强氧化性的HClO,可以杀死细菌、病毒 | |
| D. | 氯气是绿色气体,不会污染空气 |
17.将Mg、Cu组成的2.64g混合物投入适量稀硝酸中恰好反应,固体完全溶解时收集到还原产物NO气体0.896L(标准状况),向反应后溶液中加入2mol•L-1NaOH溶液60mL时金属离子恰好沉淀完全.则形成沉淀的物质的量为( )
| A. | 0.03mol | B. | 0.06mol | C. | 0.12mol | D. | 0.24mol |