题目内容
5.下列说法错误的是( )| A. | 分子式为C2H4O2的有机物不一定是乙酸 | |
| B. | 乙炔与足量Br2发生加成反应生成1,1,2,2-四溴乙烷 | |
| C. | 淀粉、蔗糖、葡萄糖在一定条件下都能发生水解反应 | |
| D. | 实验室用乙醇和浓H2SO4制备乙烯时,反应液体的温度要迅速上升到170℃ |
分析 A.分子式为C2H4O2的有机物可能为乙酸或甲酸甲酯;
B.乙炔为CH≡CH,可与溴以1:2加成;
C.葡萄糖为单糖,不能发生水解反应;
D.乙醇在170℃发生消去反应生成乙烯,在140℃发生取代反应生成乙醚.
解答 解:A.分子式为C2H4O2的有机物可能为乙酸或甲酸甲酯,则不一定为乙酸,故A正确;
B.乙炔为CH≡CH,可与溴以1:2加成,生成1,1,2,2-四溴乙烷,故B正确;
C.葡萄糖为单糖,不能发生水解反应,而淀粉、蔗糖在一定条件下都能发生水解反应,故C错误;
D.乙醇在170℃发生消去反应生成乙烯,在140℃发生取代反应生成乙醚,则用乙醇和浓H2SO4制备乙烯时,反应液体的温度要迅速上升到170℃,故D正确;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的组成、官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意常见有机物的性质,题目难度不大.

练习册系列答案
相关题目
15.下列金属防腐的措施中,使用外加电流的阴极保护法的是( )
| A. | 枪炮表面涂上一层油 | B. | 金属护拦表面涂漆 | ||
| C. | 水中的钢闸门连接电源的负极 | D. | 地下钢管连接镁块 |
16.常温下,某溶液中由水电离出的c(H+)=1×10-30 mol•L-1,该溶液中溶质不可能是( )
| A. | KHSO4 | B. | Fe2(SO4)3 | C. | KOH | D. | HNO3 |
13.高铁的快速发展方便了我们的出行.工业上用铝热反应 (2A1+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+A12O3)焊接钢轨间的缝隙.在反应中,Fe2O3( )
| A. | 是氧化剂 | B. | 是还原剂 | ||
| C. | 既是氧化剂也是还原剂 | D. | 既不是氧化剂也不是还原剂 |
20.下列反应的离子方程式中,正确的是( )
| A. | 铁和稀盐酸反应:2 Fe+6H+═2Fe3++3 H2↑ | |
| B. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 碳酸钙溶于稀盐酸中:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 碳酸氢钠溶液中滴入NaOH溶液:HCO3-+OH-═H2O+CO2↑ |
10.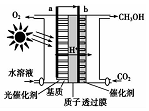 科学家最近开发了一种“叶片绿色电池”,利用CO2和H2O合成甲醇,示意图如下,关于该电池的说法正确的是( )
科学家最近开发了一种“叶片绿色电池”,利用CO2和H2O合成甲醇,示意图如下,关于该电池的说法正确的是( )
 科学家最近开发了一种“叶片绿色电池”,利用CO2和H2O合成甲醇,示意图如下,关于该电池的说法正确的是( )
科学家最近开发了一种“叶片绿色电池”,利用CO2和H2O合成甲醇,示意图如下,关于该电池的说法正确的是( )| A. | 该新型电池仅存在化学能与电能的转化 | |
| B. | 电池总反应为2CO2+4H2O=2CH3OH+3O2 | |
| C. | 电子从电极b流向电极a | |
| D. | 产生标准状况下2.24 LO2,转移电子0.6NA |
17.Na2O2、Cl2、SO2等均能使品红溶液褪色.下列说法正确的是( )
| A. | Na2O2、Cl2、SO2使品红溶液褪色原理不同 | |
| B. | Na2O2和SO2反应时,过氧化钠既作氧化剂又作还原剂 | |
| C. | 为了褪色更快,可同时向品红溶液通入等物质的量Cl2和SO2 | |
| D. | 可用H2S溶液来区别Cl2和SO2 |
14.下列物质中,既能跟盐酸反应,又能跟氢氧化钠溶液反应的是( )
| A. | NaAlO2 | B. | Al2O3 | C. | Fe2O3 | D. | AlCl3 |