题目内容
2.下列关于盐酸与醋酸两种稀溶液的说法正确的是( )| A. | 均为100mL0.1mol/L的两种溶液可中和等物质的量的氢氧化钠 | |
| B. | pH=3的两种溶液稀释100倍,pH都为5 | |
| C. | 相同浓度的两种溶液中c(H+)相同 | |
| D. | 两溶液中分别加入少量对应的钠盐,c(H+)均明显减小 |
分析 A、物质的量相等的盐酸和醋酸消耗氢氧化钠的物质的量是相等的;
B、醋酸是弱电解质存在电离平衡,盐酸是强电解质完全电离,加水稀释促进弱电解质电离
C、醋酸是弱电解质存在电离平衡,盐酸是强电解质;
D、醋酸中存在电离平衡,根据影响电离平衡移动的因素来回答.
解答 解:A、100mL 0.1mol/L的两溶液物质的量相等的,消耗氢氧化钠的物质的量是相等的,故A正确;
B、pH=3的两种溶液稀释100倍,盐酸溶液pH为5,醋酸溶液中存在电离平衡,稀释促进水解,溶液中氢离子浓度大于盐酸,溶液PH小于5,故B错误;
C、醋酸是弱电解质,盐酸是强电解质,相同浓度的两溶液中c(H+)是盐酸的大于醋酸的,故C错误;
D、醋酸中存在电离平衡,加入醋酸钠,c(H+)均明显减小,但是盐酸中加入少量的氯化钠,pH几乎不变,故D错误.
故选A.
点评 本题涉及弱电解质的电离以及电离平衡的影响因素等知识,属于综合知识的考查题,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.下列说法正确的是( )
| A. | 用酸性高锰酸钾溶液除去乙烷中混有的乙烯,从而得到纯净的乙烷气体 | |
| B. | 向溴水中加入一定量的CCl4并振荡,静置后出现分层现象,上层为橙红色溶液 | |
| C. | 除去乙酸乙酯中的乙醇和乙酸可以用烧碱溶液 | |
| D. | 油脂属于酯类物质,地沟油可用于生产肥皂或生物柴油 |
6.25℃时,有关物质的电离平衡常数如下:
(1)CH3COOH溶液中,其电离平衡常数表达式为K=$\frac{{c({H^+})•c(C{H_3}CO{O^-})}}{{c(C{H_3}COOH)}}$,常温下测得NaHSO3溶液的pH<7,其原因是HSO3-的电离程度大于其水解程度.
(2)常温下,将体积为10mLpH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者<后者(填“>”、“<”或“=”).
(3)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的关系为CO32->SO32->CH3COO->HSO3-.
(4)体积相同、c(H+)相同的①CH3COOH;②HCl;③H2SO4 三种酸溶液分别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是①>②=③(填序号).
(5)已知,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol.实验测得稀醋酸与稀NaOH溶液反应生成1mol H2O时放出57kJ的热,则醋酸溶液中,醋酸电离的热化学方程式为CH3COOH(aq)?CH3COO-(aq)+H+(aq)△H=+0.3 kJ/mol.
| 化学式 | CH3COOH | H2CO3 | H2SO3 |
| 电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(2)常温下,将体积为10mLpH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者<后者(填“>”、“<”或“=”).
(3)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的关系为CO32->SO32->CH3COO->HSO3-.
(4)体积相同、c(H+)相同的①CH3COOH;②HCl;③H2SO4 三种酸溶液分别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是①>②=③(填序号).
(5)已知,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol.实验测得稀醋酸与稀NaOH溶液反应生成1mol H2O时放出57kJ的热,则醋酸溶液中,醋酸电离的热化学方程式为CH3COOH(aq)?CH3COO-(aq)+H+(aq)△H=+0.3 kJ/mol.
10.下列装置应用于实验室进行相关实验,能达到实验目的是( )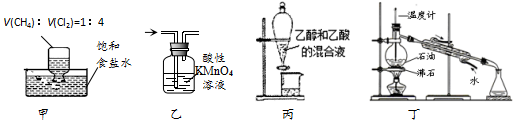

| A. | 用装置甲在光照条件下验证甲烷与氯气的反应 | |
| B. | 用装置乙除去甲烷中少量的乙烯得纯净甲烷 | |
| C. | 用装置丙分离乙醇和乙酸的混合液 | |
| D. | 用装置丁分馏石油并收集60~150℃馏分 |
7.下列实验能获得成功的是( )
| A. | 用碘水可以检验淀粉是否完全水解 | |
| B. | 苯、溴水、铁屑混合可制得溴苯 | |
| C. | 在溴乙烷中滴入AgNO3溶液可用来检验溴元素的存在 | |
| D. | 在蔗糖溶液中滴入稀硫酸加热,再滴入银氨溶液,无银镜产生,说明蔗糖没有水解 |
14.下列关于金属腐蚀与防护的说法不正确的是( )
| A. | 电化学腐蚀是造成钢铁腐蚀的主要原因 | |
| B. | 当钢铁表面水膜呈弱酸性或中性时,主要发生吸氧腐蚀正极反应为:O2-4e-+2H2O=4OH- | |
| C. | 在钢铁设施上连接比铁活泼的金属可防止钢铁腐蚀 | |
| D. | 巨型的铁制桥梁一般采用涂油漆的方法来防生锈 |
11.柠檬烯是一种食用香料,其结构简式如图所示.有关柠檬烯的分析正确的是( ) 

| A. | 它的一氯代物有8种 | |
| B. | 它和丁基苯( )互为同分异构体 )互为同分异构体 | |
| C. | 它的分子中所有的碳原子一定在同一平面上 | |
| D. | 一定条件下,它分别可以发生加成、取代、氧化、消去等反应 |
6. 如图是甲醇燃料电池的结构示意图.甲醇在催化剂作用下提供质子(H+)和电子.电子经外电路、质子经内电路到达另一极与氧气反应.电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列说法不正确的是( )
如图是甲醇燃料电池的结构示意图.甲醇在催化剂作用下提供质子(H+)和电子.电子经外电路、质子经内电路到达另一极与氧气反应.电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列说法不正确的是( )
 如图是甲醇燃料电池的结构示意图.甲醇在催化剂作用下提供质子(H+)和电子.电子经外电路、质子经内电路到达另一极与氧气反应.电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列说法不正确的是( )
如图是甲醇燃料电池的结构示意图.甲醇在催化剂作用下提供质子(H+)和电子.电子经外电路、质子经内电路到达另一极与氧气反应.电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列说法不正确的是( )| A. | 左边的电极为电池的负极,a处通入的是甲醇 | |
| B. | 每消耗3.2 g氧气转移的电子为0.4 mol | |
| C. | 电池负极的反应式为:CH3OH+H2O-6e-═CO2+6H+ | |
| D. | 电池的正极反应式为:O2+2H2O+4e-═4OH- |
 充分还原的产物与其充分催化氧化的产物发生酯化反应,其中含有一个酯基的产物种类是( )(不考虑立体异构)
充分还原的产物与其充分催化氧化的产物发生酯化反应,其中含有一个酯基的产物种类是( )(不考虑立体异构)