题目内容
14.用石墨电极电解下列溶液,阴极和阳极产生气体的体积比为2:1,其电解液pH不变的是( )| A. | NaCl | B. | H2SO4 | C. | NaOH | D. | K2SO4 |
分析 用石墨电解下列溶液,
A.电解NaCl溶液时,阳极上生成氯气、阴极上生成氢气且同时阴极附近有NaOH生成,溶液碱性增强;
B.电解稀硫酸时,阳极上生成氧气、阴极上生成氢气,实际上是电解水,导致电解后溶液c(H2SO4)增大;
C.电解NaOH溶液时,阴极上生成氢气,阳极上生成氧气,实际上是电解水,导致电解后溶液中c(NaOH)增大;
D.电解硫酸钾溶液时,阴极上生成氢气,阳极上生成氧气,实际上是电解水,导致电解后溶液中c(K2SO4)增大.
解答 解:用石墨电解下列溶液,
A.电解NaCl溶液时,阳极上生成氯气、阴极上生成氢气且同时阴极附近有NaOH生成,阴阳极上气体体积之比为1:1,溶液碱性增强,pH增大,故A错误;
B.电解稀硫酸时,阳极上生成氧气、阴极上生成氢气,阴阳极上生成气体体积之比为2:1,实际上是电解水,导致电解后溶液c(H2SO4)增大,溶液的pH减小,故B错误;
C.电解NaOH溶液时,阴极上生成氢气,阳极上生成氧气,实际上是电解水,阴阳极上生成气体体积之比为2:1,导致电解后溶液中c(NaOH)增大,溶液的pH增大,故C错误;
D.电解硫酸钾溶液时,阴极上生成氢气,阳极上生成氧气,实际上是电解水,阴阳极上生成气体体积之比为2:1,导致电解后溶液中c(K2SO4)增大,但硫酸钾溶液呈中性,溶液的pH不变,故D正确;
故选D.
点评 本题考查电解原理,为高频考点,侧重考查学生分析计算能力,明确各个电极上发生的反应、离子放电顺序是解本题关键,注意BCD实质上是电解水,注意BC电解前后溶液pH变化,题目难度不大.

练习册系列答案
相关题目
5.常温下分别将4块形状相同,质量为2.8g的铁块同时投入到下列四种溶液中,铁块首先完全溶解的是( )
| A. | 150 mL 1 mol/L盐酸 | B. | 20 mL 18.4 mol/L硫酸 | ||
| C. | 50 mL 3 mol/L盐酸 | D. | 250 mL 2 mol/L硫酸 |
19.有aXn-和bYm+两种单原子离子,它们的电子层结构相同,下列关系式或化学式不正确是( )
| A. | a+n=b-m | B. | X的氢化物化学式为HnX或XHn | ||
| C. | a<b | D. | Y的氧化物化学式为YOm |
6.下列物质属于纯净物的是( )
| A. | 酚醛树脂 | B. | 福尔马林 | C. | 葡萄糖 | D. | 纤维素 |
3.下列关于NO和NO2的叙述正确的是( )
| A. | NO是一种红棕色气体 | |
| B. | NO2与水反应生成硝酸,所以NO2是硝酸的酸酐 | |
| C. | NO和NO2是引发光化学烟雾的主要污染源 | |
| D. | NO2可用排水法收集 |
4.在25℃的条件下,下列各组离子一定能在指定环境中大量共存的是( )
| A. | pH=0的溶液中:Fe3+、Mg2+、Cl-、SO42- | |
| B. | 水电离出的c(H+)=1×10-13mol/L的溶液中:K+、HCO3-、Cl-、S2- | |
| C. | 甲基橙呈红色的溶液中:Fe3+、Na+、SO42-、CO32- | |
| D. | 在AlCl3溶液中:Na+、AlO2-、NO3-、SO42- |
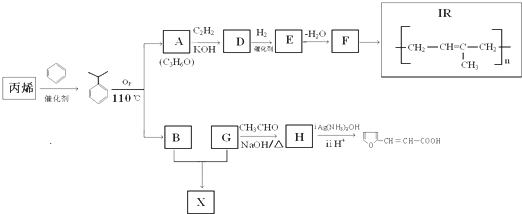
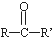 $\stackrel{KOH}{→}$
$\stackrel{KOH}{→}$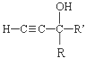
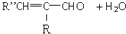 +H2O(-R、-R′、-R″表示可能相同或可能不同的原子或原子团)
+H2O(-R、-R′、-R″表示可能相同或可能不同的原子或原子团) ,反应类型是加成反应.
,反应类型是加成反应. .
. .
. .
.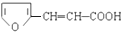 ,符合下列要求的有12种.
,符合下列要求的有12种.