题目内容
1.根据热化学方程式(在101kPa下):S(s)+O2(g)═SO2(g)△H=-297.3kJ•mol-1分析下列说法,其中不正确的是( )| A. | 该条件下32g S(s)完全燃烧放出的热量为297.23kJ | |
| B. | 反应S(g)+O2(g)═SO2(g)的△H大于-297.3kJ•mol-1 | |
| C. | 反应S(g)+O2(g)═SO2(g)的△H小于-297.3kJ•mol-1 | |
| D. | 形成1 mol SO2(g)中的化学键所释放的总能量大于断裂1 mol S(s)和1mol O2(g)中的化学键所吸收 |
分析 由S(s)+O2(g)═SO2(g)△H=-297.23kJ/mol,可知该反应为放热反应,S(s)=S(g)为吸热过程,由盖斯定律可知,S(g)+O2(g)═SO2(g)△H<-297.23kJ/mol,以此来解答.
解答 解:A.32g固体S的物质的量为1mol,由S(s)+O2(g)═SO2(g)△H=-297.23kJ/mol,所以1molS(s ) 和1molO2(g)反应生成1molSO2(g)时放出297.23kJ的热量,故A正确;
B.由盖斯定律可知,S(g)+O2(g)═SO2(g)△H<-297.23kJ/mol,故B错误;
C.由盖斯定律可知,S(g)+O2(g)═SO2(g)△H<-297.23kJ/mol,故C正确;
D.该反应为放热反应,则形成1 mol SO2的化学键所释放的总能量大于断裂1 mol S(s)和1 mol O2(g)的化学键所吸收的总能量,故D正确;
故选B.
点评 本题考查了热化学方程式的书写方法及表示的意义,明确燃烧的概念及反应热与键能、盖斯定律的关系即可解答,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列离子方程式与所述事实相符且正确的是( )
| A. | 漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| C. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| D. | 碳酸钙与醋酸溶液反应:CaCO3+2H+═Ca2++CO2↑+H2O |
9.某种玉石的主要成份是NaAlSi2O6,关于NaAlSi2O6的下列说法正确的是( )
| A. | 该物质中含有三种金属元素 | |
| B. | 该物质的一个分子中含有10个原子 | |
| C. | 该物质由四种原子直接构成 | |
| D. | 该物质中钠元素与氧元素质量比为1:6 |
16.某兴趣小组同学利用如图装置测定铁矿石样品的含量.
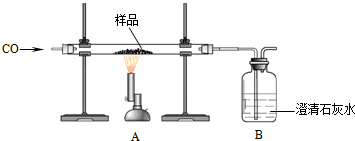
(1)A中反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe,B中的实验现象是澄清石灰水变浑浊.
(2)待充分反应后,该小组同学记录的实验数据如下:
兴趣小组同学经过讨论后认为不能选用的数据是(“装置A”或“装置B”),其理由是装置B不能将反应产生的CO2全部吸收.该铁矿石中含有氧化铁的质量分数为64%.

(1)A中反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe,B中的实验现象是澄清石灰水变浑浊.
(2)待充分反应后,该小组同学记录的实验数据如下:
| 样品质量 | 装置A中玻璃管和固体的总质量 | 装置B的质量 |
| 2.50g | 反应前55.56g | 反应前281.00g |
| 反应后55.08g | 反应后281.25g |
6.己知硫代硫酸钠溶液和稀硫酸反应可析出单质硫沉淀:Na2S2O3+H2S04═Na2SO4+S+SO2+H2O
某同学按表进行实验,请你判断哪一组先出现浑浊.
某同学按表进行实验,请你判断哪一组先出现浑浊.
| 编号 | 1 | 2 | 3 |
| 加3%Na2S2O3溶液 | 5mL | 5mL | 5mL |
| 1:5的硫酸 | 25滴 | 15滴 | 25滴 |
| 温度/℃ | 室温 | 室温+10 | 室温+20 |
| 出现浑浊的快慢 |
13.下列除去杂质的方法不正确的是( )
| A. | 镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥 | |
| B. | 用过量氨水除去Fe3+溶液中的少量Al3+ | |
| C. | 加入新制的生石灰,再加热蒸馏,可以除去乙醇中的少量水 | |
| D. | Mg(OH)2中混有少量Al(OH)3,加入足量烧碱溶液,充分反应,过滤 |
10.我国古代的有关典籍中有“银针验毒”的记载,“银针验毒”的反应原理之一是4Ag+2H2S+O2═2Ag2S+2H2O.下列有关该反应的说法正确的是( )
| A. | O2被还原 | B. | Ag是氧化剂 | C. | Ag得到电子 | D. | O2发生氧化反应 |