题目内容
A、B、C、D、E是中学化学常见的分子或离子,它们核外都有10个电子,且A是由5个原子核组成的粒子.它们之间可发生如下变化:A+B═C+D;B+E═2D,且D与大多数酸性氧化物及碱性氧化物均能反应.
(1)A的电子式: ,B的电子式: .
(2)E的化学式为: .
(3)用电子式表示D的形成过程: .
(4)实验室制取C的方程式: .
(1)A的电子式:
(2)E的化学式为:
(3)用电子式表示D的形成过程:
(4)实验室制取C的方程式:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题,化学键与晶体结构
分析:A、B、C、D、E是中学化学常见的分子或离子,它们核外都有10个电子,D与大多数酸性氧化物及碱性氧化物均能反应,则D为水,A是由5个原子核组成的粒子,则A可能为CH4或NH4+,它们之间可发生如下变化:A+B═C+D;B+E═2D,则A为NH4+,B为OH-,C为NH3,E为H3O+,据此答题;
解答:
解:A、B、C、D、E是中学化学常见的分子或离子,它们核外都有10个电子,D与大多数酸性氧化物及碱性氧化物均能反应,则D为水,A是由5个原子核组成的粒子,则A可能为CH4或NH4+,它们之间可发生如下变化:A+B═C+D;B+E═2D,则A为NH4+,B为OH-,C为NH3,E为H3O+,
(1)A为NH4+,它的电子式为 ,B为OH-,它的电子式为
,B为OH-,它的电子式为 ,
,
故答案为: ;
; ;
;
(2)由上面的分析可知,E的化学式为:H3O+,
故答案为:H3O+;
(3)D为水,用电子式表示水的形成过程为 ,
,
故答案为: ;
;
(4)实验室用氯化铵和氢氧化钙加热制取氨气,反应的方程式为Ca(OH)2+NH4CI
NH3↑+CaCI2+H2O,
故答案为:Ca(OH)2+NH4CI
NH3↑+CaCI2+H2O;
(1)A为NH4+,它的电子式为
 ,B为OH-,它的电子式为
,B为OH-,它的电子式为 ,
,故答案为:
 ;
; ;
;(2)由上面的分析可知,E的化学式为:H3O+,
故答案为:H3O+;
(3)D为水,用电子式表示水的形成过程为
 ,
,故答案为:
 ;
;(4)实验室用氯化铵和氢氧化钙加热制取氨气,反应的方程式为Ca(OH)2+NH4CI
| ||
故答案为:Ca(OH)2+NH4CI
| ||
点评:本题主要考查了10电子粒子及相关的化学用语,难度不大,解题目的关键在于熟记常见的10电子粒子和相关的反应.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列表述正确的是( )
A、NaH中氢离子结构示意图为: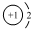 | ||||
B、NH4I的电子式: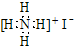 | ||||
C、质子数是82,中子数是122的铅原子:
| ||||
D、CO2的比例模型: |
下列反应中,离子方程式正确的是( )
| A、铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| B、碳酸钙跟盐酸反应:CO32-+2H+=H2O+CO2↑ |
| C、稀硫酸跟氢氧化钾溶液反应:H++OH-═H2O |
| D、氢氧化钡溶液跟稀硫酸反应:Ba2++SO42-═BaSO4↓ |
下列各组物质中,全都属于纯净物的是( )
| A、液氯和氯水 |
| B、漂白粉和乙醇 |
| C、食盐水和硫酸亚铁 |
| D、干冰和冰水混合物 |
下列说法正确的是( )
| A、HD、CaCl2、NaOH、HCl四种物质都属于化合物 |
| B、有单质参加或生成的反应一定属于氧化还原反应 |
| C、金属氧化物不一定是碱性氧化物,酸酐不一定是酸性氧化物 |
| D、金属单质只能做还原剂,非金属单质只能做氧化剂 |
下列说法正确的是( )
| A、葡萄糖能氧化新制氢氧化铜生成红色的氧化亚铜(Cu2O) |
| B、甲烷、苯、乙醇和乙酸在一定条件下都能发生取代反应 |
| C、羊毛、蚕丝、棉花和麻等天然高分子材料的主要成分都是蛋白质 |
| D、乙酸和甲酸乙酯互为同分异构体 |