题目内容
下列表述正确的是( )
A、NaH中氢离子结构示意图为: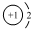 | ||||
B、NH4I的电子式: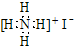 | ||||
C、质子数是82,中子数是122的铅原子:
| ||||
D、CO2的比例模型: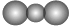 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氢离子的核电荷数为1,其最外层达到2个电子稳定结构;
B.碘离子为阴离子,电子式中需要标出其最外层电子;
C.元素符号的左上角表示质量数、左下角表示质子数,质量数=质子数+质子数;
D.比例模型中用不同体积的小球表示不同原子的大小,碳的原子半径比氧的大.
B.碘离子为阴离子,电子式中需要标出其最外层电子;
C.元素符号的左上角表示质量数、左下角表示质子数,质量数=质子数+质子数;
D.比例模型中用不同体积的小球表示不同原子的大小,碳的原子半径比氧的大.
解答:
解:A.NaH中氢离子得到一个电子,核外两个电子,结构示意图为: ,故A正确;
,故A正确;
B.NH4I为离子化合物,碘离子需要标出其最外层电子,其正确的电子式为: ,故B错误;
,故B错误;
C.质子数是82,中子数是122的铅原子的质量数为204,该原子正确表示为:82204Pb,故C错误;
D.碳和氧位于同一周期,从左到右原子半径逐渐减小,故碳的原子半径较大,CO2分子正确的比例模型为: ,故D错误;
,故D错误;
故选A.
 ,故A正确;
,故A正确;B.NH4I为离子化合物,碘离子需要标出其最外层电子,其正确的电子式为:
 ,故B错误;
,故B错误;C.质子数是82,中子数是122的铅原子的质量数为204,该原子正确表示为:82204Pb,故C错误;
D.碳和氧位于同一周期,从左到右原子半径逐渐减小,故碳的原子半径较大,CO2分子正确的比例模型为:
 ,故D错误;
,故D错误;故选A.
点评:本题考查了常见化学用语的书写判断,题目难度中等,注意掌握电子式、比例模型、离子结构示意图、元素符号等化学用语的概念及表示方法,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
下列反应中水作氧化剂的是( )
| A、2Na+2H2O═2NaOH+H2↑ |
| B、2F2+2H2O═4HF+O2↑ |
| C、SO2+H2O═H2SO3 |
| D、Cl2+H2O═HCl+HClO |
下列离子方程式,正确的是( )
| A、碳酸氢钙溶液跟盐酸反应:Ca(HCO3)2+2H+=Ca2++2H2O+2CO2↑ |
| B、Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| C、向氢氧化钡溶液中加硫酸溶液:Ba2++SO42-+H++OH-═BaSO4↓+H2O |
| D、向NaHSO4溶液中滴加少量的Ba(OH)2溶液:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
在物质分类中,前者包括后者的是( )
| A、氧化物、化合物 |
| B、化合物、非电解质 |
| C、溶液、胶体 |
| D、溶液、分散系 |
在相同物质的量的下列分子中,电子总数最少的是( )
| A、CO |
| B、O2 |
| C、H2S |
| D、NO |