题目内容
9. 2015年9月25日,我国自主研制的长征-11固体火箭成功首飞.某些固体火箭燃料中含有铝粉和硝酸钾,两者高温点火时可以发生氧化还原反应.关于该反应,下列说法正确的是( )
2015年9月25日,我国自主研制的长征-11固体火箭成功首飞.某些固体火箭燃料中含有铝粉和硝酸钾,两者高温点火时可以发生氧化还原反应.关于该反应,下列说法正确的是( )| A. | Al粉作为氧化剂 | B. | Al被氧化 | C. | Al发生还原反应 | D. | Al得到电子 |
分析 火箭燃料中含有铝粉和硝酸钾,两者高温点火时可以发生氧化还原反应,可知Al失去电子,N得到电子,以此来解答.
解答 解:A.Al失去电子作还原剂,故A错误;
B.Al失去电子被氧化,故B正确;
C.Al失去电子,被氧化,发生氧化反应,故C错误;
D.Al只能失去电子,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握习题中的信息及元素的化合价变化为解答的关键,注意金属只能失去电子,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
19.下列关于0.5mol•L-1Al2(SO4)3溶液的叙述中,不正确的是( )
| A. | Al3+与SO42-的物质的量浓度之比为2:3 | |
| B. | 1L溶液中SO42-的物质的量为1.5mol | |
| C. | 准确称取17.1g的Al2(SO4)3用100 mL蒸馏水溶解可配制得到该浓度的溶液 | |
| D. | 从1L 0.5 mol•L-1Al2(SO4)3溶液中取出100mL,Al3+浓度仍为1 mol•L-1 |
20.下列事实可证明MOH是弱碱的是( )
| A. | MOH能被醋酸中和 | |
| B. | 用MOH溶液做导电性实验,灯泡亮度较暗 | |
| C. | MOH可使酚酞试液变红 | |
| D. | 常温时0.1mol•L-1MOH溶液的pH约为11 |
17.下列有关实验,所选的装置合理的是( )
| A. | 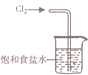 用装置吸收多余的氯气 | B. | 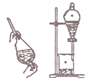 装置用酒精萃取分离水中的碘 | ||
| C. | 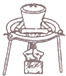 用装置除去纯碱中的小苏打 | D. |  用装置排水法收集氨气 |
4.下列过程吸收热量的是( )
| A. | 碘的升华 | B. | 天然气燃烧 | C. | 铝热反应 | D. | 钠与水反应 |
14.A、B、C、D为四种短周期主族元素,且原子序数依次增大.已知A的最外层电子数是其电子层数的2倍,B是地壳中含量最高的元素,B原子的最外层电子数是D原子最外层电子数的2倍,C原子最外层只有一个电子.下列说法正确的是( )
| A. | 原子半径:C>A | |
| B. | 气态氢化物的稳定性:A>B | |
| C. | 最髙价氧化物对应水化物的碱性:C<D | |
| D. | 元素C、D的最高价氧化物对应的水化物之间不能发生反应 |
19.等物质的量浓度、等体积的下列溶液中:①H2CO3 ②Na2CO3 ③NaHCO3 ④NH4HCO3 ⑤(NH4)2CO3.下列关系或者说法错误的是( )
| A. | c(CO32-)的大小关系为:②>⑤>③>④>① | |
| B. | 将溶液蒸干灼烧只有②能得到对应的固体物质 | |
| C. | ③④⑤既能与盐酸反应,又能与NaOH溶液反应 | |
| D. | c(HCO3-)的大小关系为:④>③>⑤>②>① |
 3,3-二乙基戊烷;
3,3-二乙基戊烷; ;
;