题目内容
9. 碳、氮及其化合物在工农业生产生活中有着重要作用.请回答下列问题:
碳、氮及其化合物在工农业生产生活中有着重要作用.请回答下列问题:(1)用CH4催化还原NOx可以消除氮氧化物的污染.例如:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2
若2mol CH4还原NO2至N2,整个过程中放出的热量为1734kJ,则△H2=-1160kJ•mol-1;
(2)据报道,科学家在一定条件下利用Fe2O3与甲烷反应可制取“纳米级”的金属铁.其反应如下:Fe2O3(s)+3CH4(g)?2Fe(s)+3CO(g)+6H2(g)△H>0
①若反应在5L的密闭容器中进行,1min后达到平衡,测得Fe2O3在反应中质量减少3.2g.则该段时间内CO的平均反应速率为0.012mol/(L•min).
②若该反应在恒温恒压容器中进行,能表明该反应达到平衡状态的是bd(选填序号)
a.CH4的转化率等于CO的产率
b.混合气体的平均相对分子质量不变
c.v(CO)与v(H2)的比值不变
d.固体的总质量不变
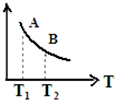
③该反应达到平衡时某物理量随温度变化如图所示,当温度由T1升高到T2时,平衡常数KA<KB(填“>”、“<”或“=”).纵坐标可以表示的物理量有哪些bc.
a.H2的逆反应速率
b.CH4的体积分数
c.混合气体的平均相对分子质量.
分析 (1)CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1 ①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2 ②
①+②得:2CH4(g)+4NO2(g)=2CO2(g)+4H2O(g)+2N2(g)根据盖斯定律以及热化学方程式的意义来解答;
(2)①结合题干计算铁物质的量,根据化学方程式定量关系计算甲烷消耗的物质的量,依据化学反应速率概念计算得到;
②反应达到平衡状态时,正逆反应速率相等,各组分浓度保持不变,据此分析;
③该反应是正反应气体体积增大的吸热反应,升温平衡正向移动,据此分析.
解答 解:(1)CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1 ①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2 ②
根据盖斯定律得:2CH4(g)+4NO2(g)=2CO2(g)+4H2O(g)+2N2(g)△H1+△H2
而 1mol CH4还原NO2至N2,整个过程中放出的热量为867kJ,所以△H1+△H2=-1734kJ•mol-1,则△H2=-1734kJ•mol-1+574kJ•mol-1=-1160 kJ•mol-1,
故答案为:-1160kJ•mol-1;
(2)①若反应在5L的密闭容器中进行,1min后达到平衡,测得Fe2O3在反应中质量减少3.2g的物质的量=$\frac{3.2g}{160g/mol}$=0.02mol,结合化学方程式,Fe2O3(s)+3CH4(g)═2Fe(s)+3CO(g)+6H2(g),计算反应的甲烷物质的量为0.06mol,则该段时间内CH4的平均反应速率=$\frac{\frac{0.06mol}{5L}}{1min}$=0.012mol/(L•min);
故答案为:0.012mol/(L•min);
②a.CH4的转化率与CO的产率与是否达到平衡状态无关,故a错误;
b.反应前后气体的物质的量和质量都不同,所以混合气体的平均相对分子质量不变说明反应达到平衡状态,故b正确;
c、v(CO)与v(H2)的比值始终不变,所以其不能说明反应达到平衡状态,故c错误;
d、固体的总质量不变,说明正逆反应速率相等,反应达到平衡状态,故d正确;
故答案为:bd;
③Fe2O3(s)+3CH4(g)═2Fe(s)+3CO(g)+6H2(g)△H>0,反应是气体体积增大的吸热反应,升温平衡正向移动,平衡常数增大,KA<KB;
a.H2的逆反应速率随温度的升高而增大,故a错误;
b.升温平衡正向移动,CH4的体积分数减小,故b正确;
c.升温平衡正向移动,混合气体的平均相对分子质量减小,故c正确;
d.升温平衡正向移动,CO的体积分数增大,故d错误;
故答案为:<;bc.
点评 本题综合考查学生有关热化学、化学反应速率和平衡的有关计算等知识,综合性较强,难度大,注意知识的迁移应用是关键.

 阅读快车系列答案
阅读快车系列答案已知:N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534kJ•mol-1,N2(g)+2O2(g)═2NO2(g)
△H=+67.7kJ•mol-1.下列关于气态肼和NO2气体反应的热化学方程式中,正确的是( )
| A. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O(l)△H=-1135.7 kJ•mol-1 | |
| B. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g)△H=-1000.3 kJ•mol-1 | |
| C. | N2H4(g)+NO2(g)═$\frac{3}{2}$N2(g)+2H2O(l)△H=-1135.7 kJ•mol-1 | |
| D. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g)△H=-1135.7 kJ•mol |
| A. | 将等体积的①、②溶液混合后,盐酸会抑制醋酸的电离,所以pH>2 | |
| B. | 将一定体积的②、③溶液混合后,溶液显碱性,则该混合溶液中c(Cl-)>c(NH4+) | |
| C. | 将一定体积的①、④溶液混合后,溶液显酸性,则V(NaOH)可能等于V(CH3COOH) | |
| D. | 向等体积的③、④溶液中加水稀释10倍,稀释后溶液中由水电离的c(H+):③>④ |
(CH3)2CHCH3(g)+$\frac{13}{2}$O2(g)═4CO2(g)+5H2O(l)△H=-2 869kJ/mol
下列说法正确的是( )
| A. | 正丁烷分子储存的能量大于异丁烷分子 | |
| B. | 正丁烷的稳定性大于异丁烷 | |
| C. | 异丁烷转化为正丁烷的过程是一个放热过程 | |
| D. | 异丁烷分子中的碳氢键比正丁烷的多 |
| A. | 室温下,46gNO2和N2O4的混合气体中含有NA个氮原子 | |
| B. | 1mol12C18O2中所含的中子数为26NA | |
| C. | 常温下,1L0.1mol/LCH3COONa溶液中含有CH3COO-和Na+总数为0.2NA | |
| D. | 常温下,1LpH=12的氨水中含有OH-的数目为0.01NA |
| A. | 用无水酒精萃取碘水中的碘 | |
| B. | Na2O2粉末加人到FeSO4溶液中.产生白色沉淀,并放出大量气泡 | |
| C. | 将浓氨水滴加到碱石灰中可制得氨气,也可用碱石灰干燥氨气 | |
| D. | 往酸性KMnO4溶液中通人SO2验证SO2的漂白性 |

 硫及其化合物有广泛应用.
硫及其化合物有广泛应用.