题目内容
7.在反应Cl2+2KBr═2KCl+Br2中,还原剂是( )| A. | Cl2 | B. | KCl | C. | Br2 | D. | KBr |
分析 Cl2+2KBr═2KCl+Br2中,Cl元素的化合价降低,Br元素的化合价升高,以此来解答.
解答 解:失电子的元素化合价升高,含有该元素的物质作还原剂,由KBr中Br的化合价由-1 价升高到0价,KBr作还原剂;Cl2中Cl的化合价降低,作氧化剂,
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化及基本概念为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
17.已知:(1)2H2(g)+O2(g)═2H2O(g);△H=a kJ•mol-1
(2)H2(g)+$\frac{1}{2}$O2(g)═H2O(g);△H=b kJ•mol-1
(3)2H2(g)+O2(g)═2H2O(l);△H=c kJ•mol-1
(4)H2(g)+$\frac{1}{2}$O2(g)═H2O(l);△H=d kJ•mol-1
下列关系式中,正确的是( )
(2)H2(g)+$\frac{1}{2}$O2(g)═H2O(g);△H=b kJ•mol-1
(3)2H2(g)+O2(g)═2H2O(l);△H=c kJ•mol-1
(4)H2(g)+$\frac{1}{2}$O2(g)═H2O(l);△H=d kJ•mol-1
下列关系式中,正确的是( )
| A. | a=2b<0 | B. | a=2c<0 | C. | c=2d>0 | D. | c>a>b |
15.下列离子的检验方法中正确的是( )
| A. | 某溶液加AgNO3溶液生成白色沉淀,说明原溶液中有Cl- | |
| B. | 某溶液加BaCl2溶液生成白色沉淀,说明原溶液中有SO42- | |
| C. | 某溶液加NaOH溶液生成蓝色沉淀,说明原溶液中有Mg2+ | |
| D. | 某溶液加NaOH溶液生成红褐色沉淀,说明原溶液中有Fe3+ |
2.下列说法正确的是( )
| A. | SiO2溶于水显酸性 | |
| B. | CO2通入水玻璃中可得到硅酸 | |
| C. | SiO2是酸性氧化物,它不溶于任何酸 | |
| D. | SiO2在常温下不与任何物质反应 |
19.下列有关合金的说法正确的是( )
| A. | 合金的硬度一般比它的成分金属大 | |
| B. | 合金的熔点一般比它的成分金属的熔点高 | |
| C. | 合金在工业上的用途比纯金属更广 | |
| D. | 生活中用量最大的合金是铁合金 |
16.1999年曾报导合成和分离了含高能量的正离子N5+的化合物N5AsF6,下列叙述错误的是( )
| A. | N5+共有34个核外电子 | |
| B. | N5+中氮氮原子间以共用电子对结合 | |
| C. | 化合物N5AsF6中As化合价为+1 | |
| D. | 化合物N5AsF6属于离子晶体 |
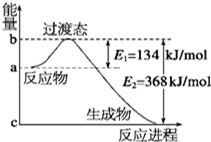 (1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)CO2(g)+NO(g)△H=-234kJ/mol.
(1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)CO2(g)+NO(g)△H=-234kJ/mol.