题目内容
有机物A易溶于水,且1molA能与Na反应生成0.5molH2,但不与NaOH溶液反应,已知A通过如下转化关系可制得化学式为C4H8O2的酯.回答下列问题.

(1)写出A的结构简式 ,其分子中含有的官能团是 (写名称).A与钠反应的化学方程式: .
(2)写出下列反应化学方程式,并在括号中注明反应类型
B→C:
C+A→D: .

(1)写出A的结构简式
(2)写出下列反应化学方程式,并在括号中注明反应类型
B→C:
C+A→D:
考点:有机物的推断
专题:有机物的化学性质及推断
分析:A可以连续发生氧化反应,则A为醇,有机物A易溶于水,且1molA能与Na反应生成0.5molH2,故A分子含有1个-OH,C与A反应得到酯E的分子式为C4H8O2,属于饱和一元酯,由转化关系可知A、B、C分子中含有碳原子数目相等,结合E的分子式可知,A、B、C分子中均含有2个含有碳原子,故A为CH3CH2OH,乙醇发生氧化反应生成B为CH3CHO,乙醛发生氧化反应生成C为CH3COOH,乙酸与乙醇发生酯化反应生成D为CH3COOCH2CH3,据此解答.
解答:
解:A可以连续发生氧化反应,则A为醇,有机物A易溶于水,且1molA能与Na反应生成0.5molH2,故A分子含有1个-OH,C与A反应得到酯E的分子式为C4H8O2,属于饱和一元酯,由转化关系可知A、B、C分子中含有碳原子数目相等,结合E的分子式可知,A、B、C分子中均含有2个含有碳原子,故A为CH3CH2OH,乙醇发生氧化反应生成B为CH3CHO,乙醛发生氧化反应生成C为CH3COOH,乙酸与乙醇发生酯化反应生成D为CH3COOCH2CH3,
(1)由上述分析可知,A的结构简式为CH3CH2OH,其分子中含有的官能团是:羟基,与钠反应的化学方程式:2CH3CH2OH+Na→2CH3CH2O Na+H2↑,
故答案为:CH3CH2OH;羟基;2CH3CH2OH+Na→2CH3CH2O Na+H2↑;
(2)B→C是乙醛发生氧化反应生成乙酸,反应方程式为:2CH3CHO+O2
2CH3COOH;
C+A→D是乙酸与乙醇发生酯化反应生成乙酸乙酯,反应方程式为:CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O,
故答案为:2CH3CHO+O2
2CH3COOH (氧化反应);CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O (酯化反应).
(1)由上述分析可知,A的结构简式为CH3CH2OH,其分子中含有的官能团是:羟基,与钠反应的化学方程式:2CH3CH2OH+Na→2CH3CH2O Na+H2↑,
故答案为:CH3CH2OH;羟基;2CH3CH2OH+Na→2CH3CH2O Na+H2↑;
(2)B→C是乙醛发生氧化反应生成乙酸,反应方程式为:2CH3CHO+O2
| Cu |
| △ |
C+A→D是乙酸与乙醇发生酯化反应生成乙酸乙酯,反应方程式为:CH3CH2OH+CH3COOH
| 浓硫酸 |
| △ |
故答案为:2CH3CHO+O2
| Cu |
| △ |
| 浓硫酸 |
| △ |
点评:本题考查有机物推断,涉及烯烃、醇、醛、羧酸的性质与转化,注意根据酯E的分子式推断,难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
分子式C4H8O2的有机物与硫酸溶液共热可得有机物A和B.将A氧化最终可得C,且B和C为同系物.若B可发生斐林反应,则原有机物的结构简式为( )
| A、HCOOCH2CH2CH3 |
| B、CH3COOCH2CH3 |
| C、CH3CH2COOCH3 |
| D、HOCH2CH2CH2CHO |
某溶液中有Fe3+、Mg2+、Fe2+和Na+四种离子,若向其中加入过量的NaOH溶液,微热并搅拌,再加入过量盐酸,溶液中大量增加的阳离子是( )
| A、Fe3+ |
| B、Mg2+ |
| C、Na+ |
| D、Fe2+ |
 ).在浓硫酸存在下,A可发生如图所示的反应.
).在浓硫酸存在下,A可发生如图所示的反应.
 工业上以铬铁矿(主要成分FeO?Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7?2H2O)的主要反应如下:
工业上以铬铁矿(主要成分FeO?Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7?2H2O)的主要反应如下: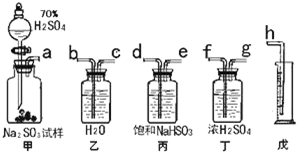 某研究性小组拟用下述方案测定一份亚硫酸钠试样的氧化变质程度.
某研究性小组拟用下述方案测定一份亚硫酸钠试样的氧化变质程度.
