题目内容
13.关于pH相同的醋酸和盐酸溶液,下列叙述不正确的是( )| A. | 两种酸溶液中c(CH3COO-)=c(Cl-) | |
| B. | 取等体积的两种酸溶液分别中和NaOH溶液,醋酸消耗NaOH的物质的量比盐酸多 | |
| C. | 取等体积的两种酸溶液分别与完全一样的足量锌粒反应,开始时反应速率盐酸大于醋酸 | |
| D. | 取等体积的两种酸溶液分别进行稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m>n |
分析 A、pH相同的醋酸和盐酸溶液,氢离子浓度相等,氢氧根离子浓度相同;
B、pH相同的醋酸和盐酸溶液,醋酸的浓度大于盐酸;
C、开始时反应速率和氢离子浓度大小有关;
D、盐酸是强酸,醋酸是弱酸,所以醋酸溶液中存在电离平衡,加水稀释能促进弱电解质电离.
解答 解:A、pH相同的醋酸和盐酸溶液,氢离子浓度相等,氢氧根离子浓度相同,根据电荷守恒,则c(CH3COO-)=c(Cl-),故A正确;
B、pH相同的醋酸和盐酸溶液,醋酸的浓度大于盐酸,等体积的两种酸溶液分别中和NaOH溶液,醋酸消耗NaOH的物质的量比盐酸多,故B正确;
C、开始时反应速率和氢离子浓度大小有关,pH相同的醋酸和盐酸溶液,开始氢离子浓度一样,所以开始反应速率一样,故C错误;
D、pH相同、体积相同的醋酸和盐酸两种溶液分别加水稀释后,促进醋酸的电离,结果两溶液的pH仍然相同,所以醋酸稀释的倍数大,即m>n,故D正确;
故选C.
点评 本题考查强弱电解质溶液,注意加水促进弱电解质电离的特点,题目难度不大.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
3.研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式,以下用于研究有机物的方法不正确的是( )
| A. | 蒸馏常用于分离提纯液态有机混合物,温度计的水银球应位于支管口附近 | |
| B. | 核磁共振氢谱通常用于分析有机物的相对分子质量 | |
| C. | 燃烧法通常是研究和确定有机物成分的有效方法之一 | |
| D. | 对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团 |
1.通常用来衡量一个国家石油化工生产发展水平的标志是( )
| A. | 石油的产量 | B. | 乙烯的产量 | C. | 汽油的产量 | D. | 硫酸的产量 |
8.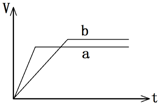 某同学在试管中用一定量的铁片与足量的稀硫酸反应,得到产生氢气的体积随时间变化的图象(b).若铁的用量不变,改变一个反应条件,得到图象(a).则改变的条件可能是( )
某同学在试管中用一定量的铁片与足量的稀硫酸反应,得到产生氢气的体积随时间变化的图象(b).若铁的用量不变,改变一个反应条件,得到图象(a).则改变的条件可能是( )
 某同学在试管中用一定量的铁片与足量的稀硫酸反应,得到产生氢气的体积随时间变化的图象(b).若铁的用量不变,改变一个反应条件,得到图象(a).则改变的条件可能是( )
某同学在试管中用一定量的铁片与足量的稀硫酸反应,得到产生氢气的体积随时间变化的图象(b).若铁的用量不变,改变一个反应条件,得到图象(a).则改变的条件可能是( )| A. | 向试管中滴加少许硫酸铜溶液 | B. | 在反应过程中对试管加热 | ||
| C. | 用铁粉代替铁片 | D. | 用98%的浓硫酸代替稀硫酸 |
18.下列物质能与金属钠作用放出气体的是( )
| A. | C2H5OH | B. | CH4 | C. | C2H4 | D. | CH3COOCH2CH3 |
5.下列有关物质性质或用途的说法不正确的是( )
| A. | 乙醇能够使蛋白质变性,75%(体积分数)的乙醇溶液可用于医疗消毒 | |
| B. | 乙二醇的水溶液凝固点很低,可用作汽车发动机的抗冻剂 | |
| C. | 光照时乙烷与氯气能发生取代反应,工业上常用该反应生产氯乙烷 | |
| D. | 乙酸( CH3COOH)与硬脂酸(C17H35COOH)互为同系物 |
2.下列叙述不能判断某化学平衡一定发生移动的是( )
| A. | 反应体系的温度改变 | |
| B. | 反应混合物中各组分的百分含量改变 | |
| C. | 正、逆反应速率改变 | |
| D. | 反应物的物质的量改变 |
3.甲~辛等元素在周期表中的位置如下表所示.下列说法正确的是( )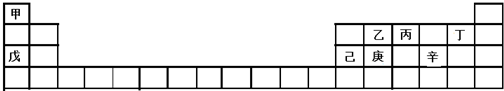

| A. | 甲、戊、己的单质都是金属 | |
| B. | 乙、丙、丁的氢化物稳定性依次增强 | |
| C. | 庚的氧化物不能和丁的氢化物反应 | |
| D. | 己的氧化物能分别与戊和辛的最高价氧化物的水化物反应 |
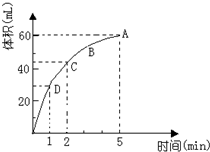 为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于 50mL密度为 1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放
为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于 50mL密度为 1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放