题目内容
3.甲~辛等元素在周期表中的位置如下表所示.下列说法正确的是( )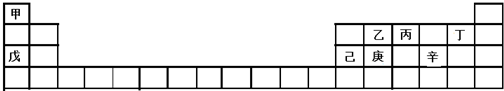
| A. | 甲、戊、己的单质都是金属 | |
| B. | 乙、丙、丁的氢化物稳定性依次增强 | |
| C. | 庚的氧化物不能和丁的氢化物反应 | |
| D. | 己的氧化物能分别与戊和辛的最高价氧化物的水化物反应 |
分析 根据元素在周期表中的位置知,甲、乙、丙、丁、戊、己、庚、辛分别是H、C、N、F、Na、Al、Si、S元素,
A、氢气都是非金属单质;
B、非金属性越强氢化物越稳定;
C、二氧化硅与氢氟酸反应生成四氟化硅;
D、铝的氧化物是两性氧化物.
解答 解:根据元素在周期表中的位置知,甲、乙、丙、丁、戊、己、庚、辛分别是H、C、N、F、Na、Al、Si、S元素,
A、氢气都是非金属单质,不全是金属,故A错误;
B、非金属性越强氢化物越稳定,所以乙、丙、丁的氢化物稳定性依次增强,故B正确;
C、二氧化硅与氢氟酸反应生成四氟化硅,故C错误;
D、铝的氧化物是两性氧化物,既能氢氧化钠,又能与硫酸反应,故D正确;
故选BD.
点评 本题主要考查的元素周期表以及根据元素在周期表中的位置确定元素,再结合元素、物质的性质分析解答,难度不大.

练习册系列答案
相关题目
13.关于pH相同的醋酸和盐酸溶液,下列叙述不正确的是( )
| A. | 两种酸溶液中c(CH3COO-)=c(Cl-) | |
| B. | 取等体积的两种酸溶液分别中和NaOH溶液,醋酸消耗NaOH的物质的量比盐酸多 | |
| C. | 取等体积的两种酸溶液分别与完全一样的足量锌粒反应,开始时反应速率盐酸大于醋酸 | |
| D. | 取等体积的两种酸溶液分别进行稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m>n |
11.如图所示的装置最适宜于收集的气体是( )
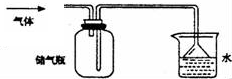

| A. | HCl | B. | NH3 | C. | NO | D. | NO2 |
18.某烃含有一个碳碳三键,与氢气发生加成反应后,产物结构简式为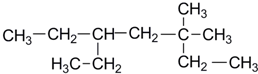 ,则该烃的可能的结构有几种( )
,则该烃的可能的结构有几种( )
 ,则该烃的可能的结构有几种( )
,则该烃的可能的结构有几种( )| A. | 4种 | B. | 3种 | C. | 2种 | D. | 1种 |
8.下列有关同分异构体数目的叙述中,正确的是( )
| A. | 碳原子数小于或等于10的烷烃中其一氯代物只有一种的烷烃有4种 | |
| B. | C8H10中只有三种属于芳香烃的同分异构体 | |
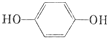
| C. | 结构简式为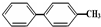 的烃,分子中含有两个苯环的该烃的同分异构体为4种 的烃,分子中含有两个苯环的该烃的同分异构体为4种 | |
| D. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有3种 |
7. 甲苯(
甲苯(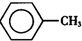 )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛(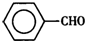 )、苯甲酸(
)、苯甲酸(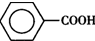 )等
)等
产品.下表列出了有关物质的部分物理性质,请回答:
注:甲苯、苯甲醛、苯甲酸三者互溶.
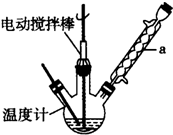
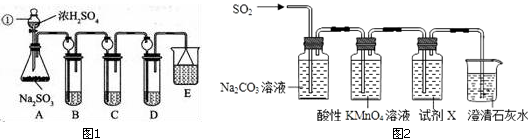
实验室可用如图装置模拟制备苯甲醛.实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸和
2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时.
(1)装置a的名称是球形冷凝管,主要作用是冷凝回流,防止甲苯挥发导致产率降低.三颈瓶中发生反应的化学方程式为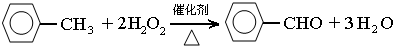 ,此反应的原子利用率理论上可达66.25%.
,此反应的原子利用率理论上可达66.25%.
(2)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是温度过高时过氧化氢分解速度加快,实际参加反应的过氧化氢质量减小,影响产量.
(3)反应完毕后,反应混合液经过自然冷却至室温时,还应经过过滤、蒸馏(填操作名称)等操作,才能得到苯甲醛粗产品.
(4)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸.
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是dacb(按步骤顺序填字母).
a.对混合液进行分液 b.过滤、洗涤、干燥
c.水层中加人盐酸调节pH=2 d.与适量碳酸氢钠溶液混合震荡
②若对实验①中获得的苯甲酸产品进行纯度测定,可称取2.500g产品,溶于200mL乙醇配成溶液,量取所得的乙醇溶液20.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000moL/KOH标准液滴定,到达滴定终点时消耗KOH溶液18.00mL.产品中苯甲酸的质量分数为87.84%.下列情况会使测定结果偏低的是ad(填字母).
a.滴定时俯视读取耗碱量 b.KOH标准液长时间接触空气
c.配置KOH标准液时仰视定容 d.将酚酞指示剂换为甲基橙溶液.
 甲苯(
甲苯( )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛( )、苯甲酸(
)、苯甲酸( )等
)等产品.下表列出了有关物质的部分物理性质,请回答:
| 名称 | 性状 | 熔点(℃) | 沸点(℃) | 相对密度(ρ水=1g/cm3) | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8660 | 不溶 | 互溶 |
| 苯甲醛 | 无色液体 | -26 | 179 | 1.0440 | 微溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 122.1 | 249 | 1.2659 | 微溶 | 易溶 |
实验室可用如图装置模拟制备苯甲醛.实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸和
2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时.
(1)装置a的名称是球形冷凝管,主要作用是冷凝回流,防止甲苯挥发导致产率降低.三颈瓶中发生反应的化学方程式为
 ,此反应的原子利用率理论上可达66.25%.
,此反应的原子利用率理论上可达66.25%.(2)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是温度过高时过氧化氢分解速度加快,实际参加反应的过氧化氢质量减小,影响产量.
(3)反应完毕后,反应混合液经过自然冷却至室温时,还应经过过滤、蒸馏(填操作名称)等操作,才能得到苯甲醛粗产品.
(4)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸.
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是dacb(按步骤顺序填字母).
a.对混合液进行分液 b.过滤、洗涤、干燥
c.水层中加人盐酸调节pH=2 d.与适量碳酸氢钠溶液混合震荡
②若对实验①中获得的苯甲酸产品进行纯度测定,可称取2.500g产品,溶于200mL乙醇配成溶液,量取所得的乙醇溶液20.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000moL/KOH标准液滴定,到达滴定终点时消耗KOH溶液18.00mL.产品中苯甲酸的质量分数为87.84%.下列情况会使测定结果偏低的是ad(填字母).
a.滴定时俯视读取耗碱量 b.KOH标准液长时间接触空气
c.配置KOH标准液时仰视定容 d.将酚酞指示剂换为甲基橙溶液.

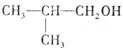 .
. .
. .
.