题目内容
4. 化学能帮助我们更好地认识生活、改善生活.
化学能帮助我们更好地认识生活、改善生活.①家用铁锅未洗净晾干,放置一段时间后出现红褐色锈斑,其主要的原因是铁发生了电化学腐蚀.
②乘车禁止携带物品的部分标识如图所示.在浓硝酸、食盐、汽油、石膏四种物品中,不能携带上车的是浓硝酸和汽油.
③过氧乙酸(
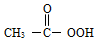 )易分解为乙酸和氧气,其稀溶常用于餐具器械的消毒.过氧乙酸分解的化学方程式2C2H4O3$\frac{\underline{\;\;△\;\;}}{\;}$2C2H4O2+O2↑.某胃药的主要成分是AlbMgc(OH)mCO3,常用于治疗胃酸过多,写出其中与胃酸反应的化学方程式2AlbMgc(OH)mCO3+(6b+4c)HCl=2bAlCl3+2cMgCl2+(3b+2c+m)H2O+2CO2↑.
)易分解为乙酸和氧气,其稀溶常用于餐具器械的消毒.过氧乙酸分解的化学方程式2C2H4O3$\frac{\underline{\;\;△\;\;}}{\;}$2C2H4O2+O2↑.某胃药的主要成分是AlbMgc(OH)mCO3,常用于治疗胃酸过多,写出其中与胃酸反应的化学方程式2AlbMgc(OH)mCO3+(6b+4c)HCl=2bAlCl3+2cMgCl2+(3b+2c+m)H2O+2CO2↑.
分析 ①铁锅中含有Fe、C,Fe、C和电解质溶液构成原电池,中性条件下,钢铁发生吸氧腐蚀;
②乘坐公共交通工具禁止携带易燃易爆、腐蚀性和有毒物品;
③过氧乙酸温度稍高即分解放出氧气并生成醋酸(C2H4O2),据此书写化学方程式;AlbMgc(OH)mCO3和盐酸反应生成AlCl3、MgCl2、H2O和CO2.
解答 解:①铁锅中含有Fe、C,Fe、C和电解质溶液构成原电池,Fe易失电子作负极而加速被腐蚀,所以铁锅的锈蚀属于电化学腐蚀,故答案为:电化学腐蚀;
②乘坐公共交通工具禁止携带易燃易爆、腐蚀性和有毒物品,而浓硝酸属于腐蚀性药品,汽油属于易燃易爆的液体,故均不能携带上车,故答案为:浓硝酸和汽油;
③过氧乙酸温度稍高即分解放出氧气并生成醋酸(C2H4O2),反应的化学方程式为:2C2H4O3$\frac{\underline{\;\;△\;\;}}{\;}$2C2H4O2+O2↑.AlbMgc(OH)mCO3是碱式碳酸盐,故能和盐酸反应生成AlCl3、MgCl2、H2O和CO2,化学方程式为2AlbMgc(OH)mCO3+(6b+4c) HCl=2b AlCl3+2cMgCl2+(3b+2c+m)H2O+2CO2↑,
故答案为:2CH3COOH→2CH3COOH+O2↑;2AlbMgc(OH)mCO3+(6b+4c) HCl=2b AlCl3+2cMgCl2+(3b+2c+m)H2O+2CO2↑.
点评 本题考查了钢铁的电化学腐蚀和化学方程式的书写,难度不大,应注意生活常识的积累以及根据已有的知识来进行知识迁移从而书写陌生的化学方程式.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
12.下列选项中不能说明硫元素的非金属性强于碳元素的是( )
| A. | 硫酸酸性强于碳酸 | |
| B. | 硫与氢气加热到500℃生成H2S,碳与氢气隔绝空气加热到1200℃生成CH4 | |
| C. | CS2中硫显示-2价 | |
| D. | 硫位于ⅥA族,碳位于ⅣA族 |
12.某研究小组为探究铁发生电化学腐蚀的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化(结果如图2).下列叙述错误的是( )


| A. | 图2中,t2时容器中压强明显小于起始压强是因为铁粉发生了吸氧腐蚀 | |
| B. | 碳粉表面的电极反应式只有:2H2O+O2+4e-═4OH- | |
| C. | 碳粉表面一定发生了还原反应 | |
| D. | 图3中,发生腐蚀时电子转移方向如箭头所示 |
9.下列说法正确的是( )
| A. | 弱电解质溶液中至少存在两种共价化合物分子 | |
| B. | 强电解质都是离子化合物,弱电解质都是共价化合物 | |
| C. | NH3属于非电解质,但其水溶液能够导电 | |
| D. | 同位素单质混合在一起一般是纯净物 |
16.下列关于物质分类的说法正确的是( )
| A. | 稀豆浆、烟水晶、氯化铁溶液都属于胶体 | |
| B. | Na2O、MgO、Mn2O7均属于碱性氧化物 | |
| C. | 氨水、冰醋酸、溴乙烷都属于弱电解质 | |
| D. | 葡萄糖、油脂、氨基酸都不属于有机高分子化合物 |
13.下列物质中,属于有机高分子材料的是( )
| A. | 不锈钢 | B. | 水泥 | C. | 橡胶 | D. | 陶瓷 |
 .
. $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$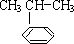
 ,取代反应.
,取代反应.