题目内容
19.22克CO2的物质的量为0.5mol,含质子的物质的量为11mol,该气体在标准状况下的体积为11.2L.分析 根据n=$\frac{m}{M}$计算出二氧化碳的物质的量,二氧化碳分子中含有22个质子,据此计算出二氧化碳含有质子的物质的量;根据V=nVm计算出标准状况下二氧化碳的体积.
解答 解:22g二氧化碳的物质的量为:$\frac{22g}{44g/mol}$=0.5mol,0.5mol二氧化碳分子中含有质子的物质的量为:0.5mol×22=11mol;
标准状况下0.5mol二氧化碳在标准状况下的体积为:22.4L/mol×0.5mol=11.2L,
故答案为:0.5;11;11.2.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、气体摩尔体积之间的关系即可解答,试题侧重基础知识的考查,有利于提高学生的 化学计算能力.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
6.向1.00L0.3mol•L-1的NaOH溶液中通入4.48L(标准状况下)CO2气体,恰好完全反应,对反应后溶液的叙述中,错误的是( )
| A. | c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | |
| B. | c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) | |
| C. | c(Na+)=c(HCO3-)+2c(CO32-)+c(OH-)-c(H+) | |
| D. | c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+) |
7.最近科学家意外发现使用碳和铜的微小尖峰可将二氧化碳和水转变为乙醇.下列有关化学用语表示错误的是( )
| A. | 中子数为34,质子数为29的铜原子:${\;}_{34}^{63}$Cu | |
| B. | 碳原子的结构示意图: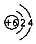 | |
| C. | 二氧化碳的电子式: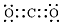 | |
| D. | 乙醇的结构简式:CH3CH2OH |
7.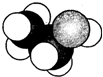 图是某有机物分子的比例模型(填充模型),其中“○”表示氢原子,“●”表示碳原子,“
图是某有机物分子的比例模型(填充模型),其中“○”表示氢原子,“●”表示碳原子,“ ”表示氧原子,该有机物的结构简式是( )
”表示氧原子,该有机物的结构简式是( )
 图是某有机物分子的比例模型(填充模型),其中“○”表示氢原子,“●”表示碳原子,“
图是某有机物分子的比例模型(填充模型),其中“○”表示氢原子,“●”表示碳原子,“ ”表示氧原子,该有机物的结构简式是( )
”表示氧原子,该有机物的结构简式是( )| A. | CH3CH3 | B. | CH2=CH2 | C. | CH3COOH | D. | CH3CH2OH |
14.配制一定体积一定浓度的NaOH溶液时,下列操作导致结果偏高的是( )
| A. | 称量NaOH固体时动作缓慢 | B. | 定容时俯视刻度线 | ||
| C. | 定容后振荡发现液面低于刻度线 | D. | 未洗涤烧杯和玻璃棒 |
17.金属钠露置在空气中会发生一系列变化,其中产物不可能是( )
| A. | Na2O2 | B. | NaOH | C. | Na2CO3•10H2O | D. | Na2CO3 |
 化学能帮助我们更好地认识生活、改善生活.
化学能帮助我们更好地认识生活、改善生活.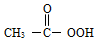 )易分解为乙酸和氧气,其稀溶常用于餐具器械的消毒.过氧乙酸分解的化学方程式2C2H4O3$\frac{\underline{\;\;△\;\;}}{\;}$2C2H4O2+O2↑.某胃药的主要成分是AlbMgc(OH)mCO3,常用于治疗胃酸过多,写出其中与胃酸反应的化学方程式2AlbMgc(OH)mCO3+(6b+4c)HCl=2bAlCl3+2cMgCl2+(3b+2c+m)H2O+2CO2↑.
)易分解为乙酸和氧气,其稀溶常用于餐具器械的消毒.过氧乙酸分解的化学方程式2C2H4O3$\frac{\underline{\;\;△\;\;}}{\;}$2C2H4O2+O2↑.某胃药的主要成分是AlbMgc(OH)mCO3,常用于治疗胃酸过多,写出其中与胃酸反应的化学方程式2AlbMgc(OH)mCO3+(6b+4c)HCl=2bAlCl3+2cMgCl2+(3b+2c+m)H2O+2CO2↑.