题目内容
3.下列有关用途的说法中,错误的是( )| A. | 液态钠可用作核反应堆的传热介质 | |
| B. | 在过渡元素中寻找半导体材料 | |
| C. | 考古时利用l4C测定一些文物的年代 | |
| D. | 235U是一种重要核燃料 |
分析 A.钠具有良好的导热性;
B.过渡元素为金属元素;
C.14C能发生衰变,用于考古;
D.235U是一种能发生核裂变的元素.
解答 解:A.钠具有良好的导热性,钠钾合金可用于作原子反应堆的导热剂,故A正确;
B.过渡元素为金属元素,都是电的量导体,应在金属与非金属分界线找半导体材料,故B错误;
C.14C能发生衰变,考古时利用l4C测定一些文物的年代,故C正确;
D.235U是一种能发生核裂变的元素,是一种核原料,故D正确;
故选:B.
点评 本题考查了元素化合物知识,侧重考查物质的性质和用途,性质决定用途,明确相关物质和元素的性质是解题关键,注意元素周期表的应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.几种短周期元素的原子半径及主要化合价如表:
下列说法正确的是( )
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10 m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
| 主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | -- |
| 最低负价 | -- | -1 | -- | -- | -3 | -2 | |
| A. | 元素X和Q形成的化合物中不可能含有共价键 | |
| B. | Y的氢化物的水溶液可用于雕刻玻璃 | |
| C. | X、Y、Z、M的单质分别与水反应,Y最剧烈 | |
| D. | R的最高价氧化物的水化物能与其气态氢化物反应生成盐 |
14.下列性质的递变规律正确的是( )
| A. | NaOH、KOH、CsOH碱性依次减弱 | |
| B. | Li、Na、K、Rb、Cs单质的失电子能力逐渐增强 | |
| C. | Li、Na、K、Rb、Cs的最外层电子数依次减小 | |
| D. | Li、Na、K、Rb、Cs电子层数相同 |
11.关于化合物的下列说法中正确的是( )
| A. | 熔化状态下不导电的化合物一定是共价化合物 | |
| B. | 只含有共价键的物质一定是共价化合物 | |
| C. | 由两种不同的原子组成的纯净物一定是化合物 | |
| D. | 不含非极性键的晶体一定是共价化合物 |
18.下列各组反应中,属于可逆反应的一组是( )
| A. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | |
| B. | NH3+CO2+H2O═NH4HCO3,NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O↑+CO2↑ | |
| C. | H2+I2$\frac{\underline{\;\;△\;\;}}{\;}$2HI,2HI$\frac{\underline{\;\;△\;\;}}{\;}$H2↑+I2↑ | |
| D. | 2Ag+Br2$\frac{\underline{\;CuO\;}}{\;}$2AgBr,2AgBr$\frac{\underline{\;光\;}}{\;}$2Ag+Br2 |
15.下列化合物中既含离子键又含共价键的是( )
| A. | 硫酸 | B. | 氯化镁 | C. | 氢氧化钡 | D. | 二氧化碳 |
13.能正确表示下列反应的离子方程式是( )
| A. | Fe3O4溶于足量稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O | |
| B. | NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O | |
| C. | 硫化钠的水解反应:S2-+H3O+HS-+H2O | |
| D. | 将0.2 mol•L-1的NH4Al(SO4)2溶液与0.3 mol•L-1的Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
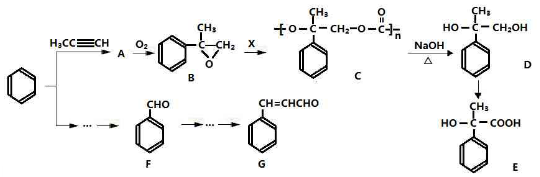
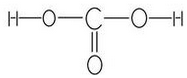 .
. .
.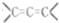 的有机物不能稳定存在)
的有机物不能稳定存在)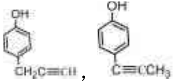 .
.