题目内容
11.几种短周期元素的原子半径及主要化合价如表:| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10 m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
| 主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | -- |
| 最低负价 | -- | -1 | -- | -- | -3 | -2 | |
| A. | 元素X和Q形成的化合物中不可能含有共价键 | |
| B. | Y的氢化物的水溶液可用于雕刻玻璃 | |
| C. | X、Y、Z、M的单质分别与水反应,Y最剧烈 | |
| D. | R的最高价氧化物的水化物能与其气态氢化物反应生成盐 |
分析 短周期元素中,Q有-2价,处于ⅥA族元素,没有正价,则Q为O元素;Y元素有+7、-1价,故Y为Cl元素;R有+5、-3价,处于ⅣA族,原子半径小于Cl,故R为N元素;X、M、Z化合价分别为+1、+2、+3价,则分别处于I族、ⅡA族、ⅢA族,且原子半径都大于氯,故X为Na、M为Mg、Z为Al,据此解答.
解答 解:短周期元素中,Q有-2价,处于ⅥA族元素,没有正价,则Q为O元素;Y元素有+7、-1价,故Y为Cl元素;R有+5、-3价,处于ⅣA族,原子半径小于Cl,故R为N元素;X、M、Z化合价分别为+1、+2、+3价,则分别处于I族、ⅡA族、ⅢA族,且原子半径都大于氯,故X为Na、M为Mg、Z为Al.
A.钠与O形成的化合物过氧化钠中存在共价键,故A错误;
B.Y为Cl,HCl的水溶液与玻璃的成分不反应,不能雕刻玻璃,故B错误;
C.X、Y、Z、M的单质分别为Na、氯气、Al、Mg,它们与水反应时,Na最剧烈,故C错误;
D.R为N元素,R的最高价氧化物的水化物能与其气态氢化物反应生成硝酸铵,属于盐,故D正确.
故选D.
点评 本题考查结构性质位置关系应用,难度不大,根据化合价及原子半径推断元素是解题关键,注意对元素周期律的理解掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.某同学写出下列烷烃的名称中,不正确的是( )
| A. | 2,3-二甲基丁烷 | B. | 3,3-二甲基丁烷 | ||
| C. | 3-甲基-3-乙基戊烷 | D. | 2,2,3,3-四甲基丁烷 |
19.下列选项属于官能团异构的是( )
①CH3CH2 CH2CH3和CH3CH(CH3)2②CH2=C(CH3)2和CH3CH=CHCH3
③CH3CH2OH和CH3OCH3 ④CH3CH2 CH2COOH 和CH3COOCH2 CH3.
①CH3CH2 CH2CH3和CH3CH(CH3)2②CH2=C(CH3)2和CH3CH=CHCH3
③CH3CH2OH和CH3OCH3 ④CH3CH2 CH2COOH 和CH3COOCH2 CH3.
| A. | ①和② | B. | ①和③ | C. | ③和④ | D. | ②和④ |
6.阿魏酸化学名称为4-羟基-3-甲氧基肉桂酸,可以做医药、保健品、化妆品原料和食品添加剂,结构简式为 ,在阿魏酸溶液中加入合适试剂(可以加热),检验其官能团,下列试剂、现象、结论都正确的是 ( )
,在阿魏酸溶液中加入合适试剂(可以加热),检验其官能团,下列试剂、现象、结论都正确的是 ( )
 ,在阿魏酸溶液中加入合适试剂(可以加热),检验其官能团,下列试剂、现象、结论都正确的是 ( )
,在阿魏酸溶液中加入合适试剂(可以加热),检验其官能团,下列试剂、现象、结论都正确的是 ( ) | 选项 | 试剂 | 现象 | 结论 |
| A | 氧化铁溶液 | 溶液变蓝色 | 它含有酚羟基 |
| B | 银氨溶液 | 产生银镜 | 它含有醛基 |
| C | 碳酸氢钠溶液 | 产生气泡 | 它含有羧基 |
| D | 溴水 | 溶液褪色 | 它含有碳碳双键 |
| A. | A | B. | B | C. | C | D. | D |
16.已知短周期元素x、y、z有如下性质:
关于短周期元素x、y、z说法错误的是( )
| 编号 | x | y | z |
| 原子半径/10-10m | 0.66 | 0.88 | 1.04 |
| 最高化合价和最低化合价 | -2 | +3 | +6 -2 |
| A. | 元素x、y位于同一周期 | |
| B. | 元素x、y、z都是非金属元素 | |
| C. | 元素z的氢化物比x的氢化物稳定 | |
| D. | 元素最高价氧化物的水化物酸性y<z |
2.下列说法中正确的是( )
| A. | 金刚石的能量比石墨高,因此金刚石比石墨更稳定 | |
| B. | 化学反应中的能量变化主要是由化学键变化引起的 | |
| C. | 浓硫酸溶于水会放出大量热,这属于放热反应 | |
| D. | 木炭需加热到一定温度时才燃烧,所以木炭燃烧是吸热反应 |
3.下列有关用途的说法中,错误的是( )
| A. | 液态钠可用作核反应堆的传热介质 | |
| B. | 在过渡元素中寻找半导体材料 | |
| C. | 考古时利用l4C测定一些文物的年代 | |
| D. | 235U是一种重要核燃料 |
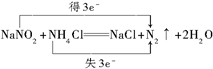 (并标出电子转移的数目和方向).
(并标出电子转移的数目和方向). 已知1-丙醇和2-丙醇的结构简式如下:
已知1-丙醇和2-丙醇的结构简式如下: .
. ,你判断的依据是因为其分子有三种不同化学环境的氢原子,所以应该有三个氢原子的吸收峰,并且符合1:1:6的峰面积比关系.
,你判断的依据是因为其分子有三种不同化学环境的氢原子,所以应该有三个氢原子的吸收峰,并且符合1:1:6的峰面积比关系.