题目内容
2013年诺贝尔化学奖授予三位美国科学家,以表彰他们在开发多尺度复杂化学系统模型方面所做的贡献.可以用量子化学计算小区间内(如光合作用叶绿体光反应时酶中、生物固氨时固氨酶中)的化学反应.
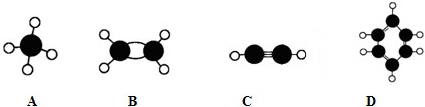
(1)固氨酶有铁蛋白和铝铁蛋白两种,它们不仅能够催化N2还原成NH3以外,还能将环境底物乙炔催化还原成乙烯,下列说法正确的有 (不定项选择).
a.C2H2、C2H4都是非极性分子
b.碳负离子CH3-呈三角锥形
c.NO+电子式为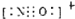
d.NH3沸点比N2高,主要是因为前者是极性分子
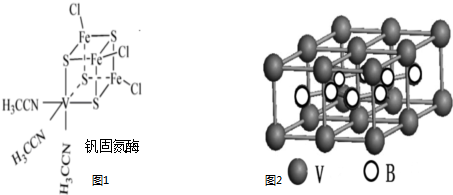
(2)钒可合成电池电极也可人工合成的二价钒(V)固氨酶(结构如图1)
①V2+基态时核外电子排布式为 .
②钒固氨酶钒的配位原子有 (写元素符号).
③熔融空气电池钒硼晶体晶胞结构如图2,该晶胞中含有钒原子数目为 .
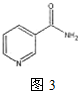
(3)烟酰胺(结构式如图3)可用于合成光合辅酶NADPH,烟酰胺分子中氨原子的杂化轨道类型有 ,lmol该分子中含σ键数目为 .
(1)固氨酶有铁蛋白和铝铁蛋白两种,它们不仅能够催化N2还原成NH3以外,还能将环境底物乙炔催化还原成乙烯,下列说法正确的有
a.C2H2、C2H4都是非极性分子
b.碳负离子CH3-呈三角锥形
c.NO+电子式为
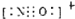
d.NH3沸点比N2高,主要是因为前者是极性分子
(2)钒可合成电池电极也可人工合成的二价钒(V)固氨酶(结构如图1)
①V2+基态时核外电子排布式为
②钒固氨酶钒的配位原子有
③熔融空气电池钒硼晶体晶胞结构如图2,该晶胞中含有钒原子数目为

(3)烟酰胺(结构式如图3)可用于合成光合辅酶NADPH,烟酰胺分子中氨原子的杂化轨道类型有

考点:晶胞的计算,原子核外电子排布,共价键的形成及共价键的主要类型,配合物的成键情况
专题:化学键与晶体结构
分析:(1)a.正负电荷重心重合的分子为非极性分子;
b.根据价层电子对互斥理论确定其空间构型;
c.NO+和氮气分子属于等电子体,等电子体结构相似;
d.NH3中氢键导致氨气熔沸点较高;
(2)①V2+基态时核外电子数是21,V是23号元素,V原子失去最外层电子生成V2+,根据构造原理书写V2+核外电子排布式;
②V含有空轨道、N原子和S原子含有孤电子对,V和N原子、S原子之间存在配位键;
③利用均摊法计算该晶胞中含有钒原子数目;
(3)环上N原子含有2个σ键和一个孤电子对,氨基上N原子含有3个σ键和1个孤电子对,据此判断N原子杂化方式,l个该分子中含σ键数目为15,据此计算lmol该分子中含σ键数目.
b.根据价层电子对互斥理论确定其空间构型;
c.NO+和氮气分子属于等电子体,等电子体结构相似;
d.NH3中氢键导致氨气熔沸点较高;
(2)①V2+基态时核外电子数是21,V是23号元素,V原子失去最外层电子生成V2+,根据构造原理书写V2+核外电子排布式;
②V含有空轨道、N原子和S原子含有孤电子对,V和N原子、S原子之间存在配位键;
③利用均摊法计算该晶胞中含有钒原子数目;
(3)环上N原子含有2个σ键和一个孤电子对,氨基上N原子含有3个σ键和1个孤电子对,据此判断N原子杂化方式,l个该分子中含σ键数目为15,据此计算lmol该分子中含σ键数目.
解答:
解:(1)a.正负电荷重心重合的分子为非极性分子,C2H2、C2H4结构对称且正负电荷重心重合,所以是非极性分子,故正确;
b.碳负离子CH3-价层电子对个数=3+
×(4+1-3×1)=4且含有一个孤电子对,所以为三角锥形,故正确;
c.NO+和氮气分子属于等电子体,等电子体结构相似,所以NO+电子式为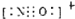 ,故正确;
,故正确;
d.NH3中含有氢键、N2中不含氢键,NH3中氢键导致氨气熔沸点较高,故错误;
故选abc;
(2)①V2+基态时核外电子数是21,V是23号元素,V原子失去最外层电子生成V2+,根据构造原理知V2+核外电子排布式为1s22s22p63s23p63d3,
故答案为:1s22s22p63s23p63d3;
②根据图知,V含有空轨道、N原子和S原子含有孤电子对,V和N原子、S原子之间存在配位键,故答案为:N、S;
③根据图片知,该晶胞中含有钒原子数目=2×
+8×
+8×
=4,故答案为:4;
(3)环上N原子含有2个σ键和一个孤电子对,氨基上N原子含有3个σ键和1个孤电子对,所以环上N原子采用sp2杂化,氨基上N原子采用杂化sp3,l个该分子中含σ键数目为15,所以lmol该分子中含σ键数目为15mol或15×6.02×1023,故答案为:sp2、sp3;15mol或15×6.02×1023.
b.碳负离子CH3-价层电子对个数=3+
| 1 |
| 2 |
c.NO+和氮气分子属于等电子体,等电子体结构相似,所以NO+电子式为
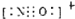 ,故正确;
,故正确;d.NH3中含有氢键、N2中不含氢键,NH3中氢键导致氨气熔沸点较高,故错误;
故选abc;
(2)①V2+基态时核外电子数是21,V是23号元素,V原子失去最外层电子生成V2+,根据构造原理知V2+核外电子排布式为1s22s22p63s23p63d3,
故答案为:1s22s22p63s23p63d3;
②根据图知,V含有空轨道、N原子和S原子含有孤电子对,V和N原子、S原子之间存在配位键,故答案为:N、S;
③根据图片知,该晶胞中含有钒原子数目=2×
| 1 |
| 2 |
| 1 |
| 4 |
| 1 |
| 8 |
(3)环上N原子含有2个σ键和一个孤电子对,氨基上N原子含有3个σ键和1个孤电子对,所以环上N原子采用sp2杂化,氨基上N原子采用杂化sp3,l个该分子中含σ键数目为15,所以lmol该分子中含σ键数目为15mol或15×6.02×1023,故答案为:sp2、sp3;15mol或15×6.02×1023.
点评:本题考查了物质结构和性质,涉及原子杂化方式的判断、核外电子排布式的书写、配位键、晶胞的计算等知识点,利用价层电子对互斥理论、构造原理、配位键概念、均摊法等知识点来分析解答,这些知识点都是考试高频点,熟练掌握这些知识解答问题.

练习册系列答案
相关题目
下列有关有机物的说法正确的是( )
| A、甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
| B、米酒变酸的过程涉及了氧化反应 |
| C、乙烯和聚丙烯都能与氢气在一定条件下发生加成反应 |
| D、淀粉、葡萄糖、脂肪和蛋白质在一定条件下都能发生水解反应 |
下列说法正确的是( )
| A、用酸性高锰酸钾即可鉴别苯酚溶液,2,4-己二烯和甲苯 |
B、按系统命名法化合物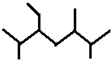 的名称为:2,5,6-三甲基-3-乙基庚烷 的名称为:2,5,6-三甲基-3-乙基庚烷 |
C、新型解热镇痛抗炎药贝诺酯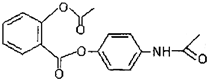 在酸性条件下完全水解可以得到3种有机物 在酸性条件下完全水解可以得到3种有机物 |
D、β-月桂烯的结构如图 ,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 ,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 |