题目内容
用下列实验装置进行相应的实验,能够达到实验目的是( )
 |  |  |  |
| A实验室制取少量的硝基苯 | B证明溴乙烷、NaOH、乙醇溶液共热生成乙烯 | C分离乙酸乙酯、碳酸钠和水的混合物 | D在实验室测定中和反应的反应热 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价,物质的分离、提纯和除杂,中和热的测定
专题:实验评价题
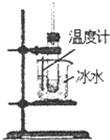
分析:A.制备硝基苯应水浴加热;
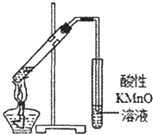
B.溴乙烷、NaOH、乙醇溶液发生消去反应生成乙烯,但乙醇挥发,乙醇也能被高锰酸钾氧化;
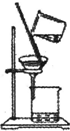
C.乙酸乙酯、碳酸钠和水的混合物,分层,乙酸乙酯在上层;
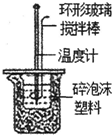
D.泡沫可防止热量散失,温度计测定反应前后的温度,玻璃搅拌棒可使反应完全反应.
B.溴乙烷、NaOH、乙醇溶液发生消去反应生成乙烯,但乙醇挥发,乙醇也能被高锰酸钾氧化;
C.乙酸乙酯、碳酸钠和水的混合物,分层,乙酸乙酯在上层;
D.泡沫可防止热量散失,温度计测定反应前后的温度,玻璃搅拌棒可使反应完全反应.
解答:
解:A.制备硝基苯应水浴加热,温度计测定水温度,加热至50℃~60℃,故A错误;
B.溴乙烷、NaOH、乙醇溶液发生消去反应生成乙烯,但乙醇挥发,乙醇也能被高锰酸钾氧化,不能说明乙烯的生成,故B错误;
C.乙酸乙酯、碳酸钠和水的混合物,分层,乙酸乙酯在上层,则利用分液法分离,不能利用过滤分离,故C错误;
D.泡沫可防止热量散失,温度计测定反应前后的温度,玻璃搅拌棒可使反应完全反应,图中中和反应的反应热测定装置合理,故D正确;
故选D.
B.溴乙烷、NaOH、乙醇溶液发生消去反应生成乙烯,但乙醇挥发,乙醇也能被高锰酸钾氧化,不能说明乙烯的生成,故B错误;
C.乙酸乙酯、碳酸钠和水的混合物,分层,乙酸乙酯在上层,则利用分液法分离,不能利用过滤分离,故C错误;
D.泡沫可防止热量散失,温度计测定反应前后的温度,玻璃搅拌棒可使反应完全反应,图中中和反应的反应热测定装置合理,故D正确;
故选D.
点评:本题考查化学实验方案的评价,为高频考点,涉及有机物的制备、混合物分离提纯、中和热测定实验等,把握反应原理及实验技能为解答的关键,侧重实验基本技能的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质在水溶液中的电离方程式书写正确的是( )
| A、NaHSO4═Na++HSO4- |
| B、NaHCO3═Na++H++CO32- |
| C、CH3COOH═H++CH3COO- |
| D、NH3?H2O?NH4++OH- |
下列有关化学用语表示正确的是( )
A、N2的电子式: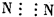 | ||
B、S2-的结构示意图: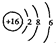 | ||
C、NH4Br的电子式: | ||
D、原子核内有l8个中子的氯原子:
|
下列各物质的名称正确的是( )
| A、1,2-二甲基丁烷 |
| B、2,3,3-三甲基-2-丁烯 |
| C、3,4,4-三甲基-1-戊炔 |
| D、2,3-二甲基苯 |
通过置换反应不可能生成( )
| A、Fe3O4 |
| B、F2 |
| C、Al2O3 |
| D、C |
同温同压下,等质量的O2和CO2相比较,下列叙述正确的是( )
| A、体积比为8:1 |
| B、分子个数之比为11:12 |
| C、物质的量之比为11:8 |
| D、原子个数之比为11:12 |
饱和的H2S溶液中,微粒浓度最大的是( )
| A、H+ |
| B、HS- |
| C、OH- |
| D、H2S |
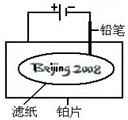 某学生设计了如图所示的“黑笔写红字”的趣味实验.滤纸上先用NaCl和无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹--“Beijing2008”. 据此,下列叙述不正确的是( )
某学生设计了如图所示的“黑笔写红字”的趣味实验.滤纸上先用NaCl和无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹--“Beijing2008”. 据此,下列叙述不正确的是( )| A、铅笔作阴极:电极反应为:2H++2e-=H2↑ | ||||
| B、铂片作阳极:电极反应为:2Cl--2e-=Cl2↑ | ||||
| C、铅笔与滤纸接触处有少量Cl2逸出 | ||||
D、上述反应总的离子方程式可表示为2Cl-+2H2O
|
关于体积相同、pH均为3的H2SO4溶液和CH3COOH溶液,下列说法正确的是( )
| A、分别与足量的Mg反应,CH3COOH溶液产生的H2多 |
| B、分别用pH=12的NaOH溶液中和,H2SO4消耗的NaOH多 |
| C、分别加入对应的钠盐固体后,二者pH仍为3 |
| D、分别加水稀释100倍后,二者的pH均变为5 |