题目内容
下列说法正确的是( )
| A、加入过量氨水,有白色沉淀生成,则原溶液一定有Al3+ |
| B、FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体剩余,加入KCSN溶液可能变成血红色 |
| C、常温下铝与浓硫酸不反应,与稀硫酸反应生成氢气 |
| D、加入NaOH溶液,产生气体使湿润的红色石蕊试纸变蓝,则原溶液一定有NH4+ |
考点:氨的化学性质,铝的化学性质,铁盐和亚铁盐的相互转变,常见阳离子的检验
专题:物质检验鉴别题,元素及其化合物
分析:A、能和氨水反应产生白色沉淀的离子有铝离子、镁离子等;
B、金属铁、铜都可以和铁离子之间发生反应;
C、常温下铝与浓硫酸之间会发生钝化;
D、铵盐可以和强碱氢氧化钠共热发生反应生成氨气,是一种碱性气体.
B、金属铁、铜都可以和铁离子之间发生反应;
C、常温下铝与浓硫酸之间会发生钝化;
D、铵盐可以和强碱氢氧化钠共热发生反应生成氨气,是一种碱性气体.
解答:
解:A、加入过量氨水,有白色沉淀生成,则原溶液可能有Al3+、Mg2+等离子中的至少一种,故A错误;
B、FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体剩余,则溶液中一定不含有铁离子,加入KCSN溶液不会变成血红色,故B错误;
C、常温下铝与浓硫酸反应,会产生钝化现象,与稀硫酸反应生成氢气,故C错误;
D、加入NaOH溶液,产生气体使湿润的红色石蕊试纸变蓝,则发生反应生成的是氨气,原溶液中一定含有铵根离子,故D正确.
故选D.
B、FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体剩余,则溶液中一定不含有铁离子,加入KCSN溶液不会变成血红色,故B错误;
C、常温下铝与浓硫酸反应,会产生钝化现象,与稀硫酸反应生成氢气,故C错误;
D、加入NaOH溶液,产生气体使湿润的红色石蕊试纸变蓝,则发生反应生成的是氨气,原溶液中一定含有铵根离子,故D正确.
故选D.
点评:本题涉及铝、铁、铜的性质、离子的检验等方面知识,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有关电解质溶液中粒子浓度关系正确的是( )
| A、pH=1的NaHSO4溶液:c(H+)═c(SO42-)十c(OH-) | ||
| B、含有AgCl和AgI固体的悬浊液:c(Ag+)>c(C1-)═c(I-) | ||
C、加水稀释CH3COONa溶液,溶液中
| ||
| D、含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)═2[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气.下列说法正确的是( )
| A、乙烧杯中放入锌的质量比甲烧杯中放入锌的质量大 |
| B、甲烧杯中的酸过量 |
| C、两烧杯中参加反应的锌等量 |
| D、反应开始后乙烧杯中的c(H+ )始终比甲烧杯中的c(H+)小 |
电子数相同的两种粒子我们称二者为等电子体.如Na+和NH4+均为10电子粒子.下列物质中,不属于C3O2的等电子体的是( )
| A、N5+ |
| B、C2NO2+ |
| C、NCN2O |
| D、NC3O- |
下列叙述正确的是( )
| A、可用浓硝酸除去铝制品表面的铜镀层 | ||
B、用催化法处理汽车尾气中的CO和NO:CO+NO
| ||
| C、浓硫酸具有吸水性,因此可用作干燥剂,能干燥氢气、硫化氢、氨气等气体 | ||
| D、因为浓硫酸在常温下不可与铁或铝反应,因此常温下可用铁制或铝制容器储存浓硫酸 |
两种硫酸溶液,一种物质的量浓度为c1,密度为ρ1;另一物质的量浓度为c2,密度为ρ2,将它们等体积混合后,所得溶液的密度为ρ3,则混合后硫酸的物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
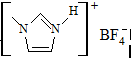 的熔点(填>、=或<),其原因是
的熔点(填>、=或<),其原因是