题目内容
下列叙述正确的是( )
| A、可用浓硝酸除去铝制品表面的铜镀层 | ||
B、用催化法处理汽车尾气中的CO和NO:CO+NO
| ||
| C、浓硫酸具有吸水性,因此可用作干燥剂,能干燥氢气、硫化氢、氨气等气体 | ||
| D、因为浓硫酸在常温下不可与铁或铝反应,因此常温下可用铁制或铝制容器储存浓硫酸 |
考点:硝酸的化学性质,氮的氧化物的性质及其对环境的影响,浓硫酸的性质
专题:元素及其化合物
分析:A、常温下,浓硫酸使Al钝化;
B、CO和NO反应是NO为氧化剂,CO为还原剂;
C、浓硫酸具有强氧化性和碱性;
D、浓硫酸在常温下使铁或铝钝化.
B、CO和NO反应是NO为氧化剂,CO为还原剂;
C、浓硫酸具有强氧化性和碱性;
D、浓硫酸在常温下使铁或铝钝化.
解答:
解:A、常温下,浓硫酸使Al钝化,Cu能溶于浓硝酸,所以可用浓硝酸除去铝制品表面的铜镀层,故A正确;
B、CO和NO反应是NO为氧化剂,N原子得电子,CO为还原剂,C原子失电子,反应的方程式为2CO+2NO
2CO2+N2;故B错误;
C、浓硫酸具有强氧化性和碱性,所以浓硫酸不能干燥碱性气体和强还原性气体,则不能干燥硫化氢、氨气,故C错误;
D、浓硫酸在常温下使铁或铝钝化,钝化是发生了氧化还原反应,故D错误.
故选A.
B、CO和NO反应是NO为氧化剂,N原子得电子,CO为还原剂,C原子失电子,反应的方程式为2CO+2NO
| 催化剂 |
C、浓硫酸具有强氧化性和碱性,所以浓硫酸不能干燥碱性气体和强还原性气体,则不能干燥硫化氢、氨气,故C错误;
D、浓硫酸在常温下使铁或铝钝化,钝化是发生了氧化还原反应,故D错误.
故选A.
点评:本题考查了浓硫酸和浓硝酸的性质,注意把握浓硫酸和浓硝酸的强氧化性,题目难度不大,侧重于基础知识的考查.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
下列叙述正确的是( )
| A、1mol/LCH3COOH与1mol/L CH3COONa溶液等体积混合,溶液中CH3COOH和CH3COO-的总数为2NA |
| B、将1molNH4NO3溶于一定浓度的稀氨水中,溶液呈中性,若不考虑挥发,溶液中一定含有NA个NH4+ |
| C、AgCl悬浊液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),往其中加入少量 NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小 |
| D、常温下,0.01mol?L-1醋酸溶液与等体积0.02 mol?L-1NaNO3溶液混合后有:2c (NO3-)═c (CH3COO-)+c (CH3COOH) |
下列说法正确的是( )
| A、加入过量氨水,有白色沉淀生成,则原溶液一定有Al3+ |
| B、FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体剩余,加入KCSN溶液可能变成血红色 |
| C、常温下铝与浓硫酸不反应,与稀硫酸反应生成氢气 |
| D、加入NaOH溶液,产生气体使湿润的红色石蕊试纸变蓝,则原溶液一定有NH4+ |
M元素的一个原子失去两个电子并转移到Y元素的两个原子中,形成离子化合物Z,下列说法不正确的是( )
| A、Z的熔点较高 |
| B、Z可以表示为M2Y |
| C、Z一定溶于水 |
| D、M形成+2价的阳离子 |
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )
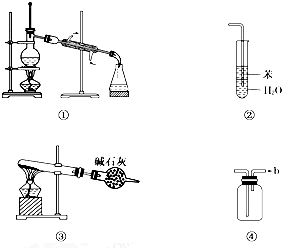

| A、装置④b口进气可收集H2、NO等气体 |
| B、装置②可用于吸收HCl气体,并防止倒吸 |
| C、以NH4HCO3为原料,装置③可用于实验室制备少量NH3 |
| D、装置①常用于分离互不相溶的液体混合物 |
下列有机反应方程式书写正确的是( )
A、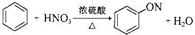 | |||
| B、H2C=CH2+Br2→CH3CHBr2 | |||
C、CH3COOH+CH3CH2OH
| |||
D、CH4+2O2
|
中和热的数值是57.3kJ/mol.下列酸、碱溶液混合产生的热量等于57.3kJ的是( )
| A、1mol/L的稀HCl溶液与1mol/L的稀NaOH溶液 |
| B、1mol/L的稀H2SO4溶液与1mol/L的稀Ba(OH)2溶液 |
| C、1L 1mol/L的稀HCl溶液与2L 1mol/L的稀NaOH溶液 |
| D、1L 1mol/L的稀H2SO4溶液与1L 1mol/L的稀Ba(OH)2溶液 |
下列不能用勒夏特列原理解释的事实是( )
| A、棕红色的NO2加压后颜色先变深后变浅 |
| B、氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深 |
| C、黄绿色的氯水光照后颜色变浅 |
| D、合成氨工业使用高压以提高氨的产量 |