题目内容
11.常温时Cu(NO3)2的水溶液呈酸(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):Cu2++2H2O?Cu(OH)2+2H+.分析 Cu(NO3)2为强酸弱碱盐,水解呈酸性,以此解答该题.
解答 解:Cu(NO3)2为强酸弱碱盐,水解呈酸性,离子方程式为Cu2++2H2O?Cu(OH)2+2H+,故答案为:酸;Cu2++2H2O?Cu(OH)2+2H+.
点评 本题考查盐类的水解,为高频考点,侧重于学生的分析能力的考查,注意把握盐类水解的规律和影响因素,难度不大.

练习册系列答案
相关题目
2.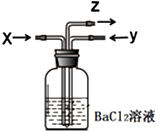 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )
 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )| A. | 洗气瓶中产生的沉淀是BaCO3 | B. | Z导管出来的气体中无CO2 | ||
| C. | 洗气瓶中产生的沉淀只有BaSO4 | D. | 洗气瓶中产生的沉淀可能有BaSO3 |
19.短周期元素M、W、X、Y、Z的原子序数依次增大,且M、W、X、Y+、Z2-的电子数与其电子层数的比值依次为1、3、4、5、6(不考虑零族元素).下列关于这些元素的叙述正确的是( )
| A. | X分别和其它四种元素均可形成至少2种化合物 | |
| B. | X、Y、Z离子半径依次增大 | |
| C. | Y和Z形成的简单离子都会破坏水的电离 | |
| D. | W、X、Z对应气态氢化物稳定性依次增强 |
16.下列物质属于电解质的是( )
| A. | 氯化钠 | B. | 铜 | C. | 氢氧化钠溶液 | D. | 乙醇 |
20.确定某无色溶液中含某离子,下列结论正确的是( )
| A. | 加 AgNO3 溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有 Cl- 存在 | |
| B. | 加 BaCl2 溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有 SO42- 存在 | |
| C. | 加盐酸,生成的气体能使澄清石灰水变浑浊,可确定有大量CO32-存在 | |
| D. | 通入 Cl2 后,溶液变为黄色,加入淀粉溶液后溶液变蓝,可确定有I- 存在 |
1.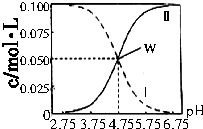 室温条件下在醋酸和醋酸钠的混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol•L-1时,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关叙述正确的是( )
室温条件下在醋酸和醋酸钠的混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol•L-1时,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关叙述正确的是( )
 室温条件下在醋酸和醋酸钠的混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol•L-1时,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关叙述正确的是( )
室温条件下在醋酸和醋酸钠的混合溶液中,当c(CH3COOH)+c(CH3COO-)=0.lmol•L-1时,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关叙述正确的是( )| A. | W点所表示的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH-) | |
| B. | pH=5.5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| C. | pH=3.5的溶液中:c(Na+)+c(H+)+c(OH-)+c(CH3COOH)=0.1mol.L-l | |
| D. | 表示CH3COO-浓度变化的是曲线Ⅰ |
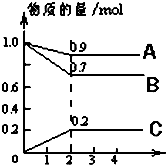 某温度时,在2L密闭容器中,A、B、C三种物质的物质的量随时间的变化曲线如图所示.由图中数据分析:
某温度时,在2L密闭容器中,A、B、C三种物质的物质的量随时间的变化曲线如图所示.由图中数据分析: