题目内容
5.下列数据大小比较不正确的是( )| A. | 沸点:H2O>H2Se>H2S | B. | 熔点:Na>Mg>Al | ||
| C. | 晶格能:NaF>NaCl>NaBr | D. | 硬度:MgO>CaO>BaO |
分析 A.同一主族元素氢化物的熔沸点随着原子序数增大而增大,但含有氢键的氢化物熔沸点最高;
B.金属的原子半径越大,离子电荷数越少,晶体的熔沸点越低;
C.离子半径越小,晶格能越大;
D.离子晶体中离子半径越小,晶格能越大,硬度越大.
解答 解:A.同一主族元素氢化物的熔沸点随着原子序数增大而增大,但含有氢键的氢化物熔沸点最高,水中含有氢键,熔沸点最高,则熔沸点H2O>H2Se>H2S,故A正确;
B.金属键越强,熔点越高,金属晶体中阳离子的电荷越多,半径越小,金属键越强,所以金属键:Na<Mg<Al,则熔点:Na<Mg<Al,故B错误;
C.离子半径Br->Cl->F-,离子半径越小,所带电荷数越大,晶格能越大,故C正确;
D.原子半径Ba>Ca>Mg,原子半径越大,键能越小,硬度越小,故D正确.
故选B.
点评 本题考查较为综合,涉及晶体的类型以及性质的判断,为高频考点,侧重于学生的分析能力的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
16.化学与生活密切相关,下列说法不正确的是( )
| A. | 做衣服用的棉和麻均与淀粉互为同分异构体 | |
| B. | 煤经过气化和液化等化学变化可转化为清洁燃料 | |
| C. | 双氧水和75%的酒精均可用于杀菌消毒,但原理不同 | |
| D. | 局部麻醉剂氯乙烷、食用植物油、鸡蛋清均可发生水解 |
13.下列说法正确的是( )
| A. | HCl溶于水能电离出H+、Cl-,所以HCl是离子化合物 | |
| B. | 碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子间的作用力 | |
| C. | He、CO2和CH4都是由分于构成,它们中都存在共价键 | |
| D. | NaHCO3受热分解生成Na2CO3、CO2和H2O,旣破坏了离子键,也破坏了共价键 |
20.下列物质中仅含有共价键的化合物是( )
| A. | N2 | B. | HCl | C. | NH4Cl | D. | NaOH |
8.下列有关物质的量的说法中,正确的是( )
| A. | CO的摩尔质量为28g | |
| B. | 32g O2含有的氧分子数为6.02×1023 | |
| C. | 标准状况下,22.4LC2H5OH的物质的量为1mol | |
| D. | 1mol•L-1NaCl溶液中含1mol Na+ |
9.下列物质的类别与所含官能团都错误的是( )
| A. | 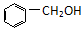 醇类-OH 醇类-OH | B. |  羧酸-COOH 羧酸-COOH | ||
| C. | 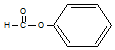 醛类-CHO 醛类-CHO | D. | CH3-O-CH3 醚类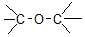 |
