题目内容
下列各反应达到化学平衡后,加压或降温都能使化学平衡向逆反应方向移动的是( )
| A、2NO2?N2O4 (正反应为放热反应) |
| B、C(s)+CO2?2CO (正反应为吸热反应) |
| C、N2+3H2?2NH3 (正反应为放热反应) |
| D、H2S?H2+S(s)(正反应为吸热反应) |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:根据化学平衡移动原理:增大压强,化学平衡向着气体体积减小的方向进行;升高温度,化学平衡向着吸热方向进行,据此结合选项解答.
解答:
解:A.正反应为体积减小的反应,增大压强,平衡正向移动,正反应是放热反应,降低温度平衡正向移动,故A不选;
B.正反应为体积增大的反应,增大压强,平衡逆向移动,正反应是吸热反应,降低温度平衡逆向移动,故B选;
C.正反应为体积减小的反应,增大压强,平衡正向移动,正反应是放热反应,降低温度平衡正向移动,故C不选;
D.反应前后体积不变,增大压强平衡不移动,正反应是吸热反应,降低温度平衡逆向移动,故D不选;
故选B.
B.正反应为体积增大的反应,增大压强,平衡逆向移动,正反应是吸热反应,降低温度平衡逆向移动,故B选;
C.正反应为体积减小的反应,增大压强,平衡正向移动,正反应是放热反应,降低温度平衡正向移动,故C不选;
D.反应前后体积不变,增大压强平衡不移动,正反应是吸热反应,降低温度平衡逆向移动,故D不选;
故选B.
点评:本题考查温度和压强对化学平衡移动的影响,注意根据反应特征利用平衡移动原理解答,难度不大.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
下列有关实验操作说法中,正确的是( )
①用pH试纸测得氯水的pH为2
②用量筒、试管胶头滴管、玻璃棒、蒸馏水和pH试纸,可鉴别pH相等的硫酸和醋酸
③在进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
④用碱式滴定管量取25.00mL溴水
⑤可用渗析的方法除去淀粉中混有的少量NaCl杂质
⑥在进行过滤操作时,为了加快速率,可用玻璃棒不断搅拌过滤器中液体.
①用pH试纸测得氯水的pH为2
②用量筒、试管胶头滴管、玻璃棒、蒸馏水和pH试纸,可鉴别pH相等的硫酸和醋酸
③在进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
④用碱式滴定管量取25.00mL溴水
⑤可用渗析的方法除去淀粉中混有的少量NaCl杂质
⑥在进行过滤操作时,为了加快速率,可用玻璃棒不断搅拌过滤器中液体.
| A、①③⑤ | B、②③⑤ |
| C、③④⑤ | D、①③④⑥ |
 已知可逆反应:mA(g)+nB(1)?pC(g).改变温度(其他条件不变)、压强(其他条件不变)对上述反应正逆反应速率的影响分别如图所示,以下叙述正确的是( )
已知可逆反应:mA(g)+nB(1)?pC(g).改变温度(其他条件不变)、压强(其他条件不变)对上述反应正逆反应速率的影响分别如图所示,以下叙述正确的是( )| A、m>p,正反应为放热反应 |
| B、m<p,正反应为吸热反应 |
| C、m+n<p,正反应为放热反应 |
| D、m+n<p,正反应为吸热反应 |
下列说法正确的是( )
| A、硅元素主要以单质、氧化物、硅酸盐的形式存在于自然界中 |
| B、浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |
| C、用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 |
| D、Ca(HCO3)2溶液与过量NaOH溶液反应可制得Ca(OH)2 |
下列物质与常用危险化学品的类别不对应的是( )
| A、浓硫酸--腐蚀品 |
| B、烧碱--剧毒品 |
| C、汽油--易燃液体 |
| D、天然气--易燃气体 |
下列判断中一定正确的是( )
| A、CaCl2及CaO2固体中阴、阳离子数之比均为2:1 |
| B、等质量的O2与O3中,氧原子的个数比为3:2 |
| C、分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1:2 |
| D、10mL 0.3mol?L-1NaCl与30mL0.1mol?L-1AlCl3溶液中Cl-物质的量浓度比为1:3 |
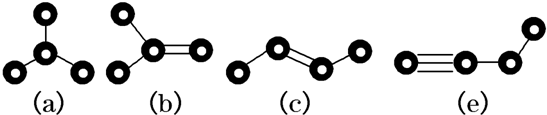
从结构上分析,有一种物质不同于其他三种,该物质是( )
A、 |
B、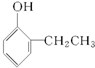 |
C、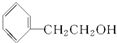 |
D、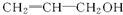 |
标准状况下,将V L A气体(摩尔质量为Mg/mol)溶于0.1L水(密度1g/cm3)中,所得溶液的密度为dg/mL,则此溶液的物质的量浓度(mol/L)为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
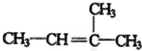 的名称是
的名称是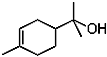 的分子式是
的分子式是