题目内容
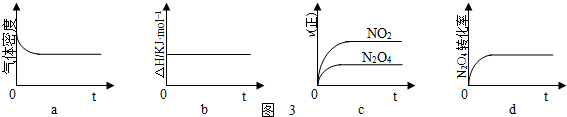
 已知可逆反应:mA(g)+nB(1)?pC(g).改变温度(其他条件不变)、压强(其他条件不变)对上述反应正逆反应速率的影响分别如图所示,以下叙述正确的是( )
已知可逆反应:mA(g)+nB(1)?pC(g).改变温度(其他条件不变)、压强(其他条件不变)对上述反应正逆反应速率的影响分别如图所示,以下叙述正确的是( )| A、m>p,正反应为放热反应 |
| B、m<p,正反应为吸热反应 |
| C、m+n<p,正反应为放热反应 |
| D、m+n<p,正反应为吸热反应 |
考点:化学反应速率与化学平衡图象的综合应用
专题:
分析:由图象可知,升高温度,逆反应速率大于正反应速率,则升高温度,平衡逆向移动;增大压强,正反应速率大于逆反应速率,则增大压强,平衡正向移动,以此来解答.
解答:
解:由图象可知,升高温度,逆反应速率大于正反应速率,则升高温度,平衡逆向移动,所以该正反应为放热反应;
增大压强,正反应速率大于逆反应速率,则增大压强,平衡正向移动,该反应为气体气体缩小的反应,所以m>p,
故选A.
增大压强,正反应速率大于逆反应速率,则增大压强,平衡正向移动,该反应为气体气体缩小的反应,所以m>p,
故选A.
点评:本题考查反应速率、化学平衡图象,明确交点为平衡点,利用温度、压强对反应速率的影响分析平衡的移动是解答本题的关键,题目难度不大.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
对于某些离子的检验及结论一定正确的是( )
| A、取样,加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| B、取样,加入硝酸银有白色沉淀,一定有Cl- |
| C、取样,加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
| D、取样,滴加KSCN溶液,不显红色,再滴加氯水后显红色,一定有Fe2+ |
在AgCl饱和溶液中尚有AgCl固体存在,当向溶液中加入0.1mol/L的盐酸时,下列说法正确的是( )
| A、AgCl沉淀溶解平衡正向移动 |
| B、AgCl溶解度增大 |
| C、溶液中c(Ag+)增大 |
| D、溶液中c(Cl-)增大 |
下列各反应达到化学平衡后,加压或降温都能使化学平衡向逆反应方向移动的是( )
| A、2NO2?N2O4 (正反应为放热反应) |
| B、C(s)+CO2?2CO (正反应为吸热反应) |
| C、N2+3H2?2NH3 (正反应为放热反应) |
| D、H2S?H2+S(s)(正反应为吸热反应) |
下列中心原子的杂化轨道类型和分子几何构型不正确的是( )
| A、H2S分子中,S为sp杂化,为直线形 |
| B、BCl3中B原子sp2杂化,为平面三角形 |
| C、CS2中C原子sp杂化,为直线形 |
| D、PCl3中P原子sp3杂化,为三角锥形 |
在水溶液中能大量共存的一组离子是( )
| A、K+、Ba2+、NO3-、Cl- |
| B、H+、Fe2+、ClO-、Cl- |
| C、Na+、Ag+、Cl-、SO42- |
| D、Al3+、Na+、HCO3-、SO42- |

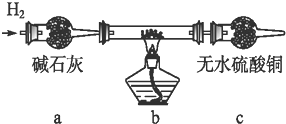 实验结束后,碳棒上的白色物质变为红色,无水硫酸铜不变色.
实验结束后,碳棒上的白色物质变为红色,无水硫酸铜不变色.