题目内容
16.常温下,下列溶液中的微粒浓度关系正确的是( )| A. | 0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合:2c(H+)-2c(OH- )=c(CH3COO-)-c(CH3COOH) | |
| B. | pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+ )>c(OH? )=c(H+) | |
| D. | 新制氯水中加入固体NaOH:c(Na+)=c(Cl- )+c(ClO- )+c(OH? ) |
分析 A.0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合得到等浓度的醋酸钠和醋酸的混合溶液,溶液中存在电荷守恒和物料守恒分析;
B.pH=8.3的NaHCO3溶液显碱性,碳酸氢根离子水解程度大于其电离程度;
C.pH=11的氨水与pH=3的盐酸等体积混合,一水合氨为弱电解质又电离出氢氧根离子,溶液显碱性;
D.溶液中一定存在电荷守恒.
解答 解:A.0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合得到等浓度的醋酸钠和醋酸的混合溶液,溶液中存在电荷守恒c(H+)+c(Na+)=c(OH- )+c(CH3COO-),物料守恒2c(Na+)=c(CH3COO-)+c(CH3COOH),得到2c(H+)-2c(OH- )=c(CH3COO-)-c(CH3COOH),故A正确;
B.pH=8.3的NaHCO3溶液显碱性,碳酸氢根离子水解程度大于其电离程度,溶液中离子浓度大小c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-),故B错误;
C.pH=11的氨水与pH=3的盐酸等体积混合,一水合氨为弱电解质又电离出氢氧根离子,溶液显碱性:c(NH4+ )>c(Cl-)>c(OH? )>c(H+),故C错误;
D.新制氯水中加入固体NaOH溶液中存在电荷守恒c(Na+)+c(H+)=c(Cl- )+c(ClO- )+c(OH? ),故D错误;
故选A.
点评 本题考查了电解质溶液中离子浓度大小、电荷守恒、物料守恒、弱电解质电离平衡等,掌握基础是解题关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.能正确表示下列反应的离子方程式的是( )
| A. | 用惰性电极电解MgCl2溶液:2Cl-+2H2O?Cl2↑+H2↑+2OH- | |
| B. | 向氯化铝溶液中滴加少量Na2CO3溶液:2Al3++3CO32-?Al2(CO3)3↓ | |
| C. | 一定量明矾溶液中滴加Ba(OH)2溶液至沉淀的质量最大时:2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O | |
| D. | FeCl3溶液与NaAlO2溶液混合:Fe3++3AlO2-?Fe(AlO2)3↓ |
4.室温下,下列说法中错误的是( )
| A. | pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-) | |
| B. | pH=5的下列溶液(①NH4Cl溶液②CH3COOH溶液;③稀盐酸)中由水电离出来的c(H+)水 ①>②>③ | |
| C. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa) | |
| D. | pH相同的下列三种溶液(①CH3COONa、②NaHCO3、③NaClO)中的c(Na+):①>②>③ |
11.下列表述中正确的是( )
| A. | 任何能使熵值增大的过程都自发进行 | |
| B. | 已知热化学方程式2SO2(g)+O2(g)?2SO3(g)△H=-Q kJ•mol-1(Q>0),则将2mol SO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量 | |
| C. | 人类利用的能源都是通过化学反应获得的 | |
| D. | 1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者放出的热量多 |
8.六种短周期元素原子序数依次增大,A和D同族,C和F同族,B、C、D、E的离子均具有相同的电子层结构,E在同周期元家中离子半径最小,A和B、C、F均能形成共价型化合物,A和B形成的化合物Y在水中呈碱性,D和F形威的化合物在水中呈中性、下列说法正确的是( )
| A. | B、C、D离子的半径大小是D>B>C | |
| B. | C的单质能将F单质从AF的溶液中置换出来 | |
| C. | 氧化物对应的水化物的酸性:B<F | |
| D. | B与C能存在F同一离子化合物中 |
6. 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:
(1)①由上表数据可知该反应为放热 (填放热,吸热,无法确定 )反应.
②下列措施能用勒夏特列原理解释是ad.(填序号)
a.增大压强有利于合成氨 b.使用合适的催化剂有利于快速生成氨
c.生产中需要升高温度至500°C左右 d.需要使用过量的N2,提高H2转化率
(2)0.2mol氨气溶于水后再与含有0.2mol硫酸的溶液反应放热QkJ,请你用热化学方程式表示其反应
式NH3.H2O(aq)+H2SO4(aq)=NH4HSO4(aq)+H2O(l)△H=-5Q kJ•mol-1.
(3)常温时,将amol氨气溶于水后,再通入bmol氯化氢,溶液体积为1L,且c(NH4+)=c(Cl-),则一水合
氨的电离平衡常数Kb=$\frac{1{0}^{-7}b}{a-b}$.(用ab表示)
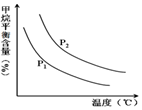
(4)原料气H2可通过反应 CH4(g)+H2O (g)?CO(g)+3H2(g) 获取,已知该反应中,当初始混合气
中的$\frac{n({H}_{2}O)}{n(C{H}_{4})}$恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
①图中,两条曲线表示压强的关系是:P1<P2
(填“>”、“=”或“<”).
②其它条件一定,升高温度,氢气的产率会增大.(填“增大”,“减小”减小,“不变”不变)
(5)原料气H2还可通过反应CO(g)+H2O(g)?CO2 (g)+H2(g) 获取.
①T℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08mol•L-1,该温度下反应的平衡常数K值为2.25.
②保持温度仍为T℃,容积体积为5L,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是cd(填序号).
a.容器内压强不随时间改变 b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6.
 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:| 温 度(℃) | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
②下列措施能用勒夏特列原理解释是ad.(填序号)
a.增大压强有利于合成氨 b.使用合适的催化剂有利于快速生成氨
c.生产中需要升高温度至500°C左右 d.需要使用过量的N2,提高H2转化率
(2)0.2mol氨气溶于水后再与含有0.2mol硫酸的溶液反应放热QkJ,请你用热化学方程式表示其反应
式NH3.H2O(aq)+H2SO4(aq)=NH4HSO4(aq)+H2O(l)△H=-5Q kJ•mol-1.
(3)常温时,将amol氨气溶于水后,再通入bmol氯化氢,溶液体积为1L,且c(NH4+)=c(Cl-),则一水合
氨的电离平衡常数Kb=$\frac{1{0}^{-7}b}{a-b}$.(用ab表示)
(4)原料气H2可通过反应 CH4(g)+H2O (g)?CO(g)+3H2(g) 获取,已知该反应中,当初始混合气
中的$\frac{n({H}_{2}O)}{n(C{H}_{4})}$恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
①图中,两条曲线表示压强的关系是:P1<P2
(填“>”、“=”或“<”).
②其它条件一定,升高温度,氢气的产率会增大.(填“增大”,“减小”减小,“不变”不变)
(5)原料气H2还可通过反应CO(g)+H2O(g)?CO2 (g)+H2(g) 获取.
①T℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08mol•L-1,该温度下反应的平衡常数K值为2.25.
②保持温度仍为T℃,容积体积为5L,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是cd(填序号).
a.容器内压强不随时间改变 b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6.

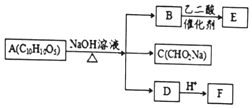 某芳香化合物A有如下转化:
某芳香化合物A有如下转化: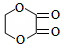 1mol F 最多消耗2mol NaOH.
1mol F 最多消耗2mol NaOH.