题目内容
4.已知某有机物的结构简式为:CH2=CHCH2CH2CH2OH,由此回答:(1)该有机物的分子式为:C5H10O;
(2)该有机物中所含的官能团的名称是:碳碳双键、羟基;
(3)写出该有机物发生加成反应的化学方程式:CH2=CHCH2CH2CH2OH+Br2→CH2BrCHBrCH2CH2CH2OH.
分析 CH2=CHCH2CH2CH2OH含有碳碳双键和醇羟基,所以应具有烯烃和醇的性质,能发生加成反应、氧化反应、酯化反应、消去反应和取代反应,以此解答该题.
解答 解:(1)由结构简式可知分子式为C5H10O,故答案为:C5H10O;
(2)由结构简式可有有机物含有碳碳双键、羟基,故答案为:碳碳双键;羟基;
(3)含有碳碳双键,可与溴水发生加成反应,方程式为CH2=CHCH2CH2CH2OH+Br2→CH2BrCHBrCH2CH2CH2OH,
故答案为:CH2=CHCH2CH2CH2OH+Br2→CH2BrCHBrCH2CH2CH2OH.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意烯烃、羧酸的性质,题目难度不大.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
14.下表是A、B、C、D四种有机物的有关信息.请根据信息回答下列问题:
(1)A中官能团的名称碳碳双键、羧基;C的结构式: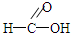 .
.
(2)B和C反应的化学方程式HCOOH+CH3CH2OH$→_{△}^{浓硫酸}$HCOOCH2CH3+H2O,其反应类型是酯化反应或取代反应.
(3)与D在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们符合通式CnH2n.当n=4时,开始出现该类有机物的同分异构体.
(4)丙烯酰胺有多种同分异构体,试写出两种分子中同时含有醛基和碳碳双键的同分异构体的结构简式:CH2=CHNHCHO、CH2=C(NH2)CHO、CH(NH2)=CHCHO.
| A | B | C | D |
| ①由C、H、O三种元素组成 ②球棍模型为:  ③能与NH3在一定条件下反应生成丙烯酰胺(CH2=CH-CONH2) | ①由C、H、O三种元素组成 ②能与Na反应,但不能与NaOH溶液反应 ③能与A反应生成相对分子质量为100的酯 | ①相对分子质量与B相同 ②能被弱氧化剂氢氧化铜氧化 ③能与NaHCO3溶液反应放出CO2气体 | ①能使溴的四氯化碳溶液褪色 ②能与水在一定条件下反应生成B |
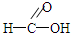 .
.(2)B和C反应的化学方程式HCOOH+CH3CH2OH$→_{△}^{浓硫酸}$HCOOCH2CH3+H2O,其反应类型是酯化反应或取代反应.
(3)与D在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们符合通式CnH2n.当n=4时,开始出现该类有机物的同分异构体.
(4)丙烯酰胺有多种同分异构体,试写出两种分子中同时含有醛基和碳碳双键的同分异构体的结构简式:CH2=CHNHCHO、CH2=C(NH2)CHO、CH(NH2)=CHCHO.
15.下列实验装置和操作正确的是( )
| A. |  测定C2H6O结构式 | B. |  验证SO2有氧化性 | ||
| C. |  实验室制氨气 | D. |  碘的CCl4溶液中分离I2 |
12.下列关于含硫化合物的叙述不正确的是( )
| A. | SO2能与CaO反应,可用生石灰作工业废气的脱硫剂 | |
| B. | SO2能使碘的淀粉溶液由蓝色变为无色,体现出漂白性 | |
| C. | 浓硫酸和Na2SO3反应制取SO2时,浓硫酸只表现酸性 | |
| D. | 医疗上曾用硫酸钡作X射线透视肠胃的内服药剂 |
2.当光束通过下列分散系时,能产生丁达尔效应的是( )
| A. | 稀豆浆 | B. | 氯化钠溶液 | C. | CuSO4溶液 | D. | KMnO4溶液 |
9.下列离子在强酸性溶液中能大量共存的一项是( )
| A. | Na+、K+、OH-、CH3COO- | B. | Na+、Ba2+、CO32-、NO3- | ||
| C. | Na+、NH4+、Cl-、HCO 3- | D. | Fe3+、K+、SO42-、NO3- |
6.赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿按一定比例混合加热可制得铜2Cu2S+Cu2O$\frac{\underline{\;\;△\;\;}}{\;}$6Cu+SO2↑.对于该反应,下列说法中正确的是( )
| A. | 该反应中的氧化剂是Cu2O | |
| B. | 氧化产物和还原产物的物质的量之比为1:6 | |
| C. | Cu既是氧化产物又是还原产物 | |
| D. | Cu2S在反应中仅做氧化剂 |
7.设NA表示阿伏加德罗常数值,下列叙述正确的是( )
| A. | 1molCl2与足量Fe反应,转移的电子数为3NA | |
| B. | 3mol NO2与足量H2O反应,转移的电子数为NA | |
| C. | 常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3NA | |
| D. | 常温常压下,11.2L甲烷含有共价键数为2NA |