题目内容
催化剂使用前必须注意 .
考点:催化剂的作用
专题:
分析:催化剂使用前注意温度、杂质、接触面积等因素分析,催化剂的活性是催化剂起催化作用的主要因素.
解答:
解:杂质能使催化剂失去催化活 性,温度.温度不能过高或过低,温度过 高会使催化剂失去催化活性,温度过低催 化活性低,接触面积. 尽可能的使催化剂接触面 积增大,这样才能达到最佳催化活性.
故答案为:杂质能使催化剂失去催化活 性,温度.温度不能过高或过低,温度过 高会使催化剂失去催化活性,温度过低催 化活性低,接触面积. 尽可能的使催化剂接触面 积增大,这样才能达到最佳催化活性.
故答案为:杂质能使催化剂失去催化活 性,温度.温度不能过高或过低,温度过 高会使催化剂失去催化活性,温度过低催 化活性低,接触面积. 尽可能的使催化剂接触面 积增大,这样才能达到最佳催化活性.
点评:本题考查了催化剂的作用理解应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下面提到的问题中,与盐的水解无关的是( )
| A、明矾和FeCl3可作净水剂 |
| B、为保存FeCl3溶液,要在溶液中加少量盐酸 |
| C、用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 |
| D、氢氟酸用塑料试剂瓶保存而不用玻璃试剂瓶保存 |
体积相同的盐酸和醋酸两种溶液,n(Cl-)=n(CH3COO-)=0.01mol,下列叙述正确的是( )
| A、醋酸溶液的pH大于盐酸 |
| B、醋酸溶液的pH小于盐酸 |
| C、与NaOH完全中和时,醋酸消耗的NaOH多于盐酸 |
| D、分别用水稀释相同倍数后,所得溶液中:n (Cl-)=n (CH3COO-) |
反应4NH3(g)+5O2=4NO(g)+6H2O(g)在一个1L的密闭容器中进行,反应30秒后,水蒸气的物质的量增加了0.45mol,则在这30秒内此反应的平均速率υ(X)可表示为( )
| A、υ(H2O)=0.45 mol?L-1?s-1 |
| B、υ(O2)=0.010 mol?L-1?s-1 |
| C、υ(NO)=0.010 mol?L-1?s-1 |
| D、υ(NH3)=0.10 mol?L-1?s-1 |
下列不属于氧化还原反应的是( )
| A、Cl2 与水反应 |
| B、Fe和水蒸气反应 |
| C、Na和水反应 |
| D、SO3和水反应 |
下列离子方程式书写正确的是( )
| A、Na2CO3溶液中滴加醋酸:CO32-+2H+=H2O+CO2↑ |
| B、Fe和FeCl3溶液:Fe+Fe3+=2 Fe2+ |
| C、AlCl3溶液中加入氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| D、H2SO4溶液和Ba(OH)2溶液:SO42-+Ba2+=BaSO4↓ |
在给定的四种溶液中,含有以下各种微粒,一定能大量共存的是( )
| A、饱和Na2CO3溶液中:NH4+、C6H5OH、NO3-、NH3?H2O |
| B、常温下葡萄糖溶液中:SCN-、Cl-、K+、NH4+ |
| C、溴水中:Na+、CO32-、NH4+、SO42- |
| D、pH大于7的溶液:Na+、Ba2+、SO32-、ClO- |
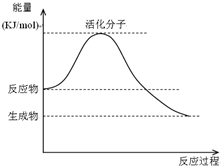 (1)如图是某化学反应中的能量变化图.
(1)如图是某化学反应中的能量变化图.