题目内容
以下关于原子的未成对电子数的叙述正确的是( )
①钠、铝、氯:1个;②硅、硫:2个;③磷:3个;④铁:4个.
①钠、铝、氯:1个;②硅、硫:2个;③磷:3个;④铁:4个.
| A、只有①③ | B、只有①②③ |
| C、只有②③④ | D、有①②③④ |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:根据能量最低原理、保里不相容原理和洪特规则写出各元素原子的电子排布式,再根据原子的电子排布式分析.
解答:
解:①钠原子的电子排布式为:1s22s22p63s1,则Na原子的未成对电子数为1;铝原子的电子排布式为:1s22s22p63s23p1,则铝原子的未成对电子数为1;氯原子的电子排布式为:1s22s22p63s23p5,则氯原子的未成对电子数为1,故①正确;
②硅原子的电子排布式为:1s22s22p63s23p2,则硅原子的未成对电子数为2;硫原子的电子排布式为:1s22s22p63s23p4,则硫原子的未成对电子数为2,故②正确;
③磷原子的电子排布式为:1s22s22p63s23p3,则磷原子的未成对电子数为3,故③正确;
④Fe的电子排布式为1s22s22p63s23p63d64s2,则铁原子的未成对电子数为4,故④正确;
故选D.
②硅原子的电子排布式为:1s22s22p63s23p2,则硅原子的未成对电子数为2;硫原子的电子排布式为:1s22s22p63s23p4,则硫原子的未成对电子数为2,故②正确;
③磷原子的电子排布式为:1s22s22p63s23p3,则磷原子的未成对电子数为3,故③正确;
④Fe的电子排布式为1s22s22p63s23p63d64s2,则铁原子的未成对电子数为4,故④正确;
故选D.
点评:本题考查了原子的未成对电子数的判断,注意根据原子电子排布式分析,题目难度不大.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、0.1mol N2与足量的H2反应,转移的电子数是0.6NA |
| B、常温下,0.1mol?L-1 NH4NO3溶液中含有的氮原子数是0.2NA |
| C、常温常压下,3.2g O2和3.2g O3所含氧原子数都是0.2NA |
| D、2.24L CO和CO2的混合气体中所含的碳原子数为0.1N A |
下列实验操作不正确的是( )
| A、分液时,分液漏斗中上层液体应从漏斗口倒出 |
| B、蒸馏时,温度计水银球靠近蒸馏烧瓶支管口 |
| C、滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面 |
| D、蒸发时,当蒸发到剩有少量液体时,停止加热,利用余热将液体蒸干 |
在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g),所得实验数据如表:
下列说法正确的是( )
| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| ④ | 900 | 0.10 | 0.15 | b |
| A、实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,用N表示的平均反应速率v(N)=1.0×10-2mol/(L?min) |
| B、实验②中,该反应的平衡常数K=2.0 |
| C、实验③中,达到平衡时,X的转化率为60% |
| D、实验④中,达到平衡时,b>0.060 |
化学与科技、生产、生活密切相关.下列说法不正确的是( )
| A、工业上,用焦炭在高温下还原二氧化硅制得粗硅 |
| B、“玉兔号”月球车太阳能电池帆板的材料是二氧化硅 |
| C、地沟油的主要成分是油脂,其组成与汽油、煤油不相同 |
| D、钠可把钛、锆、铌、钽等金属从它们的熔融的卤化物里还原出来 |
等质量的铁屑和锌粒与足量的同浓度的稀硫酸反应,下列图象可能正确的是( )
A、 |
B、 |
C、 |
D、 |
短周期主族元素X、Y、Z、W的原子序数依次增大,X的原子半径比Y的小,X与W同主族,Y、Z族序数之和为11,Z原子最外层电子数是内层电子总数的3倍.下列说法不正确的是( )
| A、元素Z、W的简单离子的电子层结构相同 |
| B、元素Y的简单气态氢化物的热稳定性比Z的弱 |
| C、由X、Y、Z三种元素形成化合物,其水溶液可能显碱性 |
| D、W、Z两种元素形成的化合物中肯定不含共价键 |
化学与环境、材料、信息、能源关系密切,下列说法错误的是( )
| A、半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
| B、将“地沟油”制成肥皂,可以提高资源的利用率 |
| C、我国首艘航母“辽宁舰”上用于舰载机降落的拦阻索是特种钢缆,属于金属材料 |
| D、推广以植物秸秆为原料的综合利用技术,避免焚烧秸秆造成空气污染 |
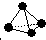 ,已知断裂1mol N-N键吸收167kJ的热量,生成1mol N≡N键放出942kJ热量.试判断相同条件下N4与N2的稳定性顺序是:
,已知断裂1mol N-N键吸收167kJ的热量,生成1mol N≡N键放出942kJ热量.试判断相同条件下N4与N2的稳定性顺序是: