题目内容
13. 在T℃时,将一定量A加入到体积为2L的某密闭容器中,发生以下化学反应:2A(g)?B(g)+C(g)△H=-akJ/mol.反应在第15min时达到平衡,反应过程中B、A的浓度比与时间t有如图所示关系,若测得第15min时c(B)=0.8mol/L,下列结论正确的是( )
在T℃时,将一定量A加入到体积为2L的某密闭容器中,发生以下化学反应:2A(g)?B(g)+C(g)△H=-akJ/mol.反应在第15min时达到平衡,反应过程中B、A的浓度比与时间t有如图所示关系,若测得第15min时c(B)=0.8mol/L,下列结论正确的是( )| A. | 反应达平衡时,A的转化率为80% | |
| B. | A的初始物质的量为2mol | |
| C. | 反应到达平衡时,放出的热量是2a KJ | |
| D. | 15min时,v正=v逆=0 |
分析 15min时达到平衡,若测得第15min时c(B)=0.8mol/L,由图可知,纵坐标为c(B)与c(A)的比,15min时比值为2,可知c(A)=0.4mol,则
2A(g)?B(g)+C(g)
开始 n 0 0
转化 1.6 0.8 0.8
平衡 0.4 0.8 0.8
A.转化率=$\frac{转化的量}{开始的量}$×100%;
B.结合n=cV计算;
C.物质的量与热量成正比;
D.平衡时,正逆反应速率相等,为动态平衡.
解答 解:15min时达到平衡,若测得第15min时c(B)=0.8mol/L,由图可知,纵坐标为c(B)与c(A)的比,15min时比值为2,可知c(A)=0.4mol,则
2A(g)?B(g)+C(g)
开始 n 0 0
转化 1.6 0.8 0.8
平衡 0.4 0.8 0.8
A.反应达平衡时,A的转化率为$\frac{1.6}{1.6+0.4}$×100%=80%,故A正确;
B.A的初始物质的量为2L×(1.6+0.4)mol/L=4mol,故B错误;
C.由热化学方程式可知,2molA反应放出热量为akJ,则反应到达平衡时,放出的热量是1.6mol/L×2L×$\frac{a}{2}$ kJ=1.6akJ,故C错误;
D.15min时,为平衡状态,则v正=v逆≠0,故D错误;
故选A.
点评 本题考查物质的量浓度随时间变化曲线,为高频考点,把握图中浓度的变化、平衡三段法为解答的关键,侧重分析与应用能力的考查,注意选项C为易错点,题目难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 下列各组物质中,不满足如图所示转化关系的是(反应条件略去,箭头表示一步转化)( )
下列各组物质中,不满足如图所示转化关系的是(反应条件略去,箭头表示一步转化)( )| 选项 | 甲 | 乙 | 丙 | 戊 |
| A | NH3 | Cl2 | N2 | H2 |
| B | C | SiO2 | CO | CuO |
| C | Al(OH)3 | NaOH | NaAlO2 | CO2 |
| D | Br2 | FeI2 | FeBr2 | Cl2 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 大于 | B. | 等于 | C. | 小于 | D. | 不能确定 |
| A. | 溴苯中的溴(氢氧化钠溶液,蒸馏) | |
| B. | 乙酸乙酯中少量的乙醇和乙酸(氢氧化钠溶液,分液) | |
| C. | 乙烷中的乙烯(酸性KMnO4溶液,洗气) | |
| D. | 乙醇中的水 (CaO,蒸馏) |
 BHT是一种常用的食品抗氧化剂,从
BHT是一种常用的食品抗氧化剂,从 出发合成BHT的方法有如下两种.下列说法错误的是( )
出发合成BHT的方法有如下两种.下列说法错误的是( )| A. | 方法一的反应类型是加成反应 | |
| B. | 推测BHT在水中的溶解度小于苯酚 | |
| C. | BHT与 都能使酸性KMnO4褪色 都能使酸性KMnO4褪色 | |
| D. | 从原子经济角度分析方法二优于方法一 |
 ,以下关于它的叙述正确的是( )
,以下关于它的叙述正确的是( )| A. | 其一氯代物有2种 | B. | 其二氯代物有5种 | ||
| C. | 其分子式为C10H14 | D. | 它常温下为气态 |
| A. | 0.64g | B. | 1.28g | C. | 2.56g | D. | 5.12g |
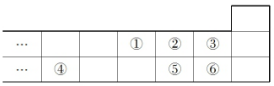
| A. | 最高价氧化物对应水化物的酸性:⑥>⑤ | |
| B. | 气态氢化物的稳定性:⑤>② | |
| C. | 元素的简单离子半径大小:④>⑤>② | |
| D. | 元素的最高正化合价:③=⑥ |
