题目内容
13.下列实验装置不合理的是( )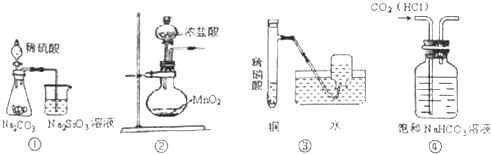
| A. | 图①可证明酸性强弱:H2SO4>H2CO3>H2SiO3 | |
| B. | 图②可用于实验室制备少量氯气 | |
| C. | 图③可用于实验室制备少量NO气体 | |
| D. | 图④可除去CO2中少量HCl气体 |
分析 A.强酸能制取弱酸;
B.浓盐酸与二氧化锰需要加热才反应;
C.稀硝酸和铜反应生成NO;
D.除去CO2中的HCl气体,选择试剂为饱和碳酸氢钠溶液.
解答 解:A.强酸能制取弱酸,酸性:H2SO4>H2CO3>H2SiO3,故A正确;
B.浓盐酸与二氧化锰需要加热才反应,常温下不反应,故B错误;
C.稀硝酸和铜反应生成NO,NO不溶于水,可用排水法收集,故C正确;
D.除去CO2中的HCl气体,选择试剂为饱和碳酸氢钠溶液,HCl与碳酸氢钠反应生成二氧化碳,故D正确.
故选B.
点评 本题考查较为综合,涉及基础实验操作,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的方法、步骤和使用的仪器,注重相关基础知识的积累,难度不大.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
4. 利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.
利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.
已知:①CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.2kJ•mol-1
②CO(g)+H2O(g)?CO2(g)+H2(g)△H=-42.3kJ•mol-1
(1)甲烷和水蒸气生成二氧化碳和氢气的热化学方程式CH4(g)+2H2O(g)=4H2(g)+CO2(g)△H=+163.9 kJ/mol.
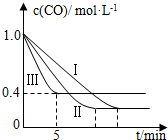
(2)为了探究反应条件对反应CO(g)+H2O(g)?CO2(g)+H2(g)△H=-42.3kJ•mol-1的影响,某活动小组设计了三个实验,实验曲线如图所示.
①请依据实验曲线图补充完整表格中的实验条件:X=530℃,Y=5MPa.
②实验Ⅲ从开始至平衡,其平均反应速度率v (CO)=0.12mol•L-1•min-1.
③实验Ⅱ达平衡时CO的转化率大于 实验Ⅲ达平衡时CO的转化率(填“大于”、“小于”或“等于”).
④在530℃时,平衡常数K=1,若往1L容器中投入0.2mol CO(g)、0.2mol H2O(g)、1mol CO2(g)、0.1mol H2(g),此时化学反应将向逆方向(填“向正方向”、“向逆方向”或“不”) 移动.
 利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.
利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.已知:①CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.2kJ•mol-1
②CO(g)+H2O(g)?CO2(g)+H2(g)△H=-42.3kJ•mol-1
(1)甲烷和水蒸气生成二氧化碳和氢气的热化学方程式CH4(g)+2H2O(g)=4H2(g)+CO2(g)△H=+163.9 kJ/mol.
(2)为了探究反应条件对反应CO(g)+H2O(g)?CO2(g)+H2(g)△H=-42.3kJ•mol-1的影响,某活动小组设计了三个实验,实验曲线如图所示.
| 编号 | 温度 | 压强 | c始(CO) | c始(H2O) |
| Ⅰ | 530℃ | 3MPa | 1.0mol•L-1 | 3.0mol•L-1 |
| Ⅱ | X | Y | 1.0mol•L-1 | 3.0mol•L-1 |
| Ⅲ | 630℃ | 5MPa | 1.0mol•L-1 | 3.0mol•L-1 |
②实验Ⅲ从开始至平衡,其平均反应速度率v (CO)=0.12mol•L-1•min-1.
③实验Ⅱ达平衡时CO的转化率大于 实验Ⅲ达平衡时CO的转化率(填“大于”、“小于”或“等于”).
④在530℃时,平衡常数K=1,若往1L容器中投入0.2mol CO(g)、0.2mol H2O(g)、1mol CO2(g)、0.1mol H2(g),此时化学反应将向逆方向(填“向正方向”、“向逆方向”或“不”) 移动.
8.下列生活中常见物质的俗名与化学式相对应的是( )
| A. | 生石灰-Ca(OH)2 | B. | 重晶石-BaCO3 | C. | 绿矾-CuSO4•5H2O | D. | 小苏打-NaHCO3 |
18.下列实验过程中,始终无明显现象的是( )
| A. | SO3通入BaCl2溶液中 | B. | CO2通入CaCl2溶液中 | ||
| C. | NH3通入MgCl2溶液中 | D. | Cl2通入KI淀粉溶液中 |
5.氯气是一种有毒气体,在运输和储存过程中必须防止泄露.若储存液氯的钢瓶发生泄露,立即采取的措施中错误的是( )
| A. | 将人群向低处疏散 | B. | 将人群逆风向疏散 | ||
| C. | 用浸有水的毛巾捂住口鼻 | D. | 向泄露地点撒一些石灰 |
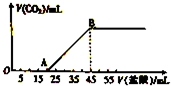 将5.08g由Na2CO3和NaHCO3组成的固体混合物完全溶于水,制成溶液,然后向该溶液中逐滴加入2mol?L-1的盐酸,所加入盐酸的体积与产生CO2体积(标准状况)的关系如图所示.
将5.08g由Na2CO3和NaHCO3组成的固体混合物完全溶于水,制成溶液,然后向该溶液中逐滴加入2mol?L-1的盐酸,所加入盐酸的体积与产生CO2体积(标准状况)的关系如图所示. 的链节为
的链节为 .其单体的结构简式分别为
.其单体的结构简式分别为 、
、 .
.