题目内容
对于反应中的能量变化,下列说法正确的是( )
| A、碳酸钙受热分解,其生成物总能量高于反应物总能量 |
| B、断开化学键的过程会放出能量 |
| C、加热才能发生的反应一定是吸热反应 |
| D、氧化反应均为吸热反应 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、碳酸钙受热分解是吸热反应;
B、断裂化学键需要吸收能量;
C、反应吸热还是放热决定与反应物与生成物的能量高低,与反应条件无关;
D、反应吸热还是放热决定与反应物与生成物的能量高低,与反应类型无关.
B、断裂化学键需要吸收能量;
C、反应吸热还是放热决定与反应物与生成物的能量高低,与反应条件无关;
D、反应吸热还是放热决定与反应物与生成物的能量高低,与反应类型无关.
解答:
解:A、碳酸钙受热分解是吸热反应,反应物总能量低于生成物,故A正确;
B、断裂化学键需要吸收能量,故B错误;
C、燃烧都是放热反应,但需要加热到着火点,故C错误;
D、燃烧都是氧化反应,并且都是放热反应,故D错误;
故选A.
B、断裂化学键需要吸收能量,故B错误;
C、燃烧都是放热反应,但需要加热到着火点,故C错误;
D、燃烧都是氧化反应,并且都是放热反应,故D错误;
故选A.
点评:本题考查了放热反应和吸热反应与反应条件无关,决定于反应物和生成物能量高低,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在周期表中短周期主族元素X、Y、Z、W,它们的原子序数依次增大.X与Z同主族,X与Z的原子序数之和为24.W原子的最外层电子数比Y原子的最外层电子数多2个.下列叙述正确的是( )
| A、气态氢化物的稳定性 Y>X |
| B、最高价氧化物的水化物酸性 Y>Z |
| C、Z的氧化物不止一种 |
| D、原子半径 Z>Y |
下列说法正确的是( )
| A、元素周期律是元素原子核外电子排布周期性变化的结果 |
| B、HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 |
| C、第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| D、形成离子键的阴阳离子间只存在静电吸引力 |
对相同状况下的NO和N2两种气体,下列说法中不正确的是( )
| A、若质量相等,则分子数相等 |
| B、若原子数相等,则分子数相等 |
| C、若分子数相等,则体积相等 |
| D、若体积相等,则原子数相等 |
2013年1月10日起一连数日我国中东部地区浓雾弥漫,能见度很低,给人们的出行带来了极大的不便.浓雾中小水滴的直径范围是( )
| A、小于1nm |
| B、在1nm~100nm之间 |
| C、大于100nm |
| D、无法确定 |
若1mol有机物A在稀H2SO4作用下水解成2mol B,下列物质中符合题意的物质A可能是( )
①蔗糖 ②麦芽糖 ③葡萄糖 ④淀粉 ⑤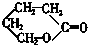 ⑥
⑥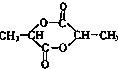 ⑦
⑦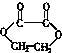 ⑧
⑧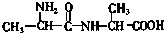
①蔗糖 ②麦芽糖 ③葡萄糖 ④淀粉 ⑤
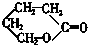 ⑥
⑥ ⑦
⑦ ⑧
⑧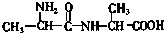
| A、①②③ | B、④⑤⑧ |
| C、②⑥⑧ | D、①⑤⑦ |
反应A+B═2C,在反应过程中,断裂1mol A中的化学键消耗的能量为Q1kJ,断裂1mol B中的化学键消耗的能量为Q2kJ,形成1mol C中的化学键释放的能量为Q3kJ;1mol A所含化学能为E1kJ,1mol B所含化学能E2kJ,1molC 所含化学能E3kJ.下列说法中一定正确的是( )
| A、若Q1+Q2<Q3,则反应为放热反应 |
| B、若Q1+Q2>Q3,则反应为放热反应 |
| C、若E1+E2>E3,则反应为放热反应 |
| D、若E1+E2>E3,则反应为吸热反应 |
已知2FeCl3+2KI=2FeCl2+2KCl+I2,H2S+I2=2HI+S,下列叙述正确的是( )
| A、氧化性Fe3+>I2>S |
| B、氧化性I2>S>Fe3+ |
| C、还原性Fe2+>I->H2S |
| D、还原性Fe2+>H2S>I- |