题目内容
反应A+B═2C,在反应过程中,断裂1mol A中的化学键消耗的能量为Q1kJ,断裂1mol B中的化学键消耗的能量为Q2kJ,形成1mol C中的化学键释放的能量为Q3kJ;1mol A所含化学能为E1kJ,1mol B所含化学能E2kJ,1molC 所含化学能E3kJ.下列说法中一定正确的是( )
| A、若Q1+Q2<Q3,则反应为放热反应 |
| B、若Q1+Q2>Q3,则反应为放热反应 |
| C、若E1+E2>E3,则反应为放热反应 |
| D、若E1+E2>E3,则反应为吸热反应 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:据△H=反应物键能和-生成物键能和=生成物能量和-反应物能量和,△H>0时反应吸热,△H<0时反应放热,据此解答.
解答:
解:△H=反应物键能和-生成物键能和=生成物能量和-反应物能量和=Q1+Q2-2Q3=2E3-E1-E2,
A、Q1+Q2<Q3则,Q1+Q2<2Q3,△H<0反应放热,故A正确;
B、Q1+Q2>Q3,不一定Q1+Q2>2Q3,故B错误;
C、E1+E2>E3,不一定E1+E2>2E3,故C错误;
D、E1+E2>E3,可能E1+E2>2E3,故D错误;
故选A.
A、Q1+Q2<Q3则,Q1+Q2<2Q3,△H<0反应放热,故A正确;
B、Q1+Q2>Q3,不一定Q1+Q2>2Q3,故B错误;
C、E1+E2>E3,不一定E1+E2>2E3,故C错误;
D、E1+E2>E3,可能E1+E2>2E3,故D错误;
故选A.
点评:本题考查了△H=反应物键能和-生成物键能和=生成物能量和-反应物能量和,题目难度不大.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
下列化学用语正确的是( )
A、NH3分子的电子式: |
B、CH4分子的比例模型: |
| C、乙醇的结构简式:CH3CH2OH |
D、K+离子的结构示意图: |
下列有关化学用语使用正确的是( )
A、硫离子的结构示意图: | ||
B、NH4Cl的电子式: | ||
C、原子核内有10个中子的氧原子:
| ||
D、Na2O2的电子式为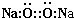 |
对于反应中的能量变化,下列说法正确的是( )
| A、碳酸钙受热分解,其生成物总能量高于反应物总能量 |
| B、断开化学键的过程会放出能量 |
| C、加热才能发生的反应一定是吸热反应 |
| D、氧化反应均为吸热反应 |
硅橡胶主要成分的结构为 ,它是由二氯二甲基硅烷
,它是由二氯二甲基硅烷 经两步反应制成的.这两步反应是( )
经两步反应制成的.这两步反应是( )
 ,它是由二氯二甲基硅烷
,它是由二氯二甲基硅烷 经两步反应制成的.这两步反应是( )
经两步反应制成的.这两步反应是( )| A、消去、加聚 |
| B、水解、缩聚 |
| C、氧化、缩聚 |
| D、水解、加聚 |
设NA表示阿伏加德罗常数的值,下列说法不正确的是( )
A、某气体的摩尔质量为ag/mol,则1个这种气体分子的质量为
| ||
| B、10g氖含有的原子数为0.5NA | ||
| C、在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10NA | ||
| D、CO和N2为等电子体,22.4L的CO气体与lmol N2所含的电子数相等 |
大米中含有丰富的维生素B1、B2,应怎样淘米营养素损失少?( )
| A、用热水烫洗 |
| B、浸泡后再流水冲洗 |
| C、用力搓洗 |
| D、根据米的清洁程度适当清洗 |
