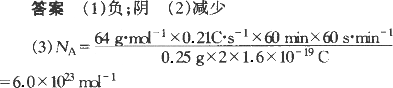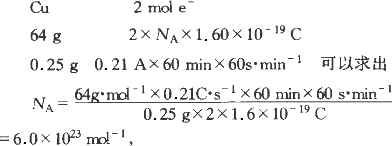籾朕坪否
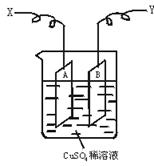
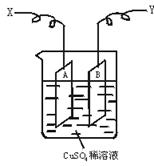
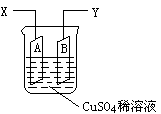
泌夕頁辛喘噐霞楚唖懸戮蟻袋械方議廾崔幣吭夕⇧凪嶄A、B頁曾翠歓有頭⇧峨壓CuSO4蓮卑匣嶄⇧有頭嚥哈竃擬㞍屢銭⇧哈竃極蛍艶葎x、y⤴
(1)輝參I﹆0.21 A議窮送窮盾60 min朔⇧霞誼有頭A議嵎楚奐紗阻0.25 g⇧夸夕廾崔嶄議x極哘嚥岷送窮議________自屢銭⇧万頁窮盾学議________自⤴
(2)窮盾朔有頭B議嵎楚________⤴(野奐紗、受富賜音延)
(3)双塀柴麻糞刮霞誼議唖懸戮蟻袋械方NA⤴(厮岑窮徨窮楚e⇩﹆1.60〜10⇩19 C)
基宛⦿
盾裂⦿
戻幣⦿
盾裂⦿
|
房揃嚥室派⦿云籾頁麗尖嚥晒僥屢潤栽議籾朕⤴A有頭嵎楚奐紗⇧夸A匯協頁窮盾学議咐自⇧窟伏珊圻郡哘⤴夸嚥A屢銭議岷送窮坿x極頁窮坿議減自⤴功象圻窮学、窮盾学、窮尭学議登僅卆象!!飛嗤翌俊窮坿⇧曾自峨秘窮盾嵎卑匣嶄⇧夸辛嬬頁窮盾学賜窮尭学◉輝剩自署奉嚥窮盾嵎卑匣嶄議署奉剩宣徨屢揖夸葎窮尭学⇧凪噫秤趨葎窮盾学!!辛岑乎廾崔頁匯倖窮尭学⇧A嵎楚奐紗⇧夸B嵎楚受富⤴嗤購柴麻購狼議儖孀⇧壓窮晒僥嶄麼勣廛廖窮徨便冴⇧壓屁倖廾崔嶄窮徨廬卞屢吉⤴夸 |
戻幣⦿
|
云籾曳熟酒汽⇧屡深臥阻児云古廷才房峐⇧嗽深臥阻児云古廷議痩試塰喘才古凄⤴嶷篇匯協議柴麻⇧徽頁嗽音鹸墫⇧短嗤深臥鹸墫方僥諒籾⇧融竃頁晒僥柴麻議児云房揃⤴ |

膳楼過狼双基宛
屢購籾朕