题目内容
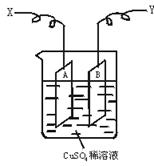
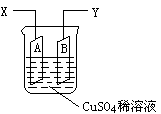
如图是可用于测量阿伏加德罗常数的装置示意图,其中A、B是两块纯铜片,插在CuSO4稀溶液中,铜片与引出导线相连,引出端分别为X、Y。
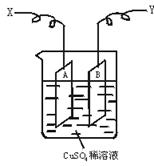
(1)当以I=0.21 A的电流电解60 min后,测得铜片A的质量增加了0.25 g,则图装置中的X端应与直流电的__________极相连,它是电解池的__________极。
(2)电解后铜片B的质量__________。(答“增加”“减少”或“不变”)
(3)列式计算实验测得的阿伏加德罗常数NA。(已知电子电量e=1.60×10-19C)
(1)负 阴 (2)减少
![]()
=6.0×1023 mol-1
解析:
因为铜片A的质量增加,A为电解池的阴极,Cu2++2e-===Cu,X端应与直流电的负极相连接。铜片B则为电解池的阳极:Cu-2e-===Cu2+,其质量减少。

练习册系列答案
相关题目