题目内容
下列离子在溶液中能大量共存的是( )
| A、Mg2+、H+、SO42-、Cl- |
| B、Ca2+、H+、NO3-、CO32- |
| C、Fe3+、Na+、SCN-、OH- |
| D、Cu2+、NH4+、Cl-、OH- |
考点:离子共存问题
专题:
分析:根据离子之间不能结合生成沉淀、气体、水、弱电解质等,不能结合生成络离子,则离子大量共存,以此来解答.
解答:
解:A.该组离子之间不反应,可大量共存,故A正确;
B.Ca2+、CO32-结合生成沉淀,H+、CO32-结合生成水和气体,则不能大量共存,故B错误;
C.Fe3+、OH-结合生成沉淀,Fe3+、SCN-结合生成络离子,不能大量共存,故C错误;
D.Cu2+、OH-结合生成沉淀,NH4+、OH-结合生成弱电解质,不能大量共存,故D错误;
故选A.
B.Ca2+、CO32-结合生成沉淀,H+、CO32-结合生成水和气体,则不能大量共存,故B错误;
C.Fe3+、OH-结合生成沉淀,Fe3+、SCN-结合生成络离子,不能大量共存,故C错误;
D.Cu2+、OH-结合生成沉淀,NH4+、OH-结合生成弱电解质,不能大量共存,故D错误;
故选A.
点评:本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应、络合反应的离子共存考查,题目难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
用分液漏斗可以分离的一组混合物是( )
| A、碘和乙醇 | B、丙醇和乙二醇 |
| C、溴苯和水 | D、甘油和水 |
在恒温恒容条件下,将4molA和2molB放入一密闭容器中2A(g)+B(g)?2C(g)+D(s),达到平衡时,C的体积分数为a;在相同条件下,按下列配比分别投放A、B、C、D,达到平衡时,C的体积分数不等于a的是( )
| A、4mol、2mol、0mol、2mol |
| B、2mol、1mol、2mol、2mol |
| C、2mol、1mol、2mol、1mol |
| D、2mol、1mol、0mol、1mol |
某化合物由碳、氢、氧三种元素组成,其红外光谱图有C-H键、H-O键、C-O键的振动吸收,该有机物的相对分子质量是60,则该有机物的结构简式可能是( )
| A、CH3CH2CH2OH |
B、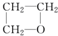 |
| C、CH3CH2OCH3 |
| D、CH3CH2CHO |
下列关于电解质溶液的叙述正确的是( )
| A、常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
| B、将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C、中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D、常温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
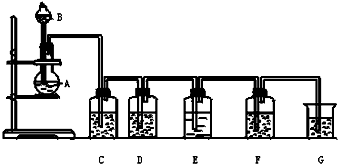 实验室用如图所示装置制备氯气(加热装置略去),并进行氯气性质实验,请回答下列问题:
实验室用如图所示装置制备氯气(加热装置略去),并进行氯气性质实验,请回答下列问题: