题目内容
11.乙醇和乙酸是生活中两种常见的有机物.下列说法正确的是( )| A. | 乙醇、乙酸都能与金属钠反应 | |
| B. | 乙醇、乙酸都能与NaOH溶液反应 | |
| C. | 乙醇、乙酸都能使紫色石蕊试液变红色 | |
| D. | 乙醇、乙酸互为同分异构体 |
分析 乙醇含-OH、乙酸含-COOH,二者均与Na反应,但乙醇与NaOH、石蕊均不反应,且二者分子式不同,以此来解答.
解答 解:A.均与Na反应生成氢气,故A正确;
B.只有乙酸与NaOH发生中和反应,故B错误;
C.只有乙酸能使紫色石蕊试液变红色,故C错误;
D.乙醇中含6个H、1个O,而乙酸中含4个H、2个O,分子式不同,不互为同分异构体,故D错误;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意醇、羧酸的性质,题目难度不大.

练习册系列答案
相关题目
1.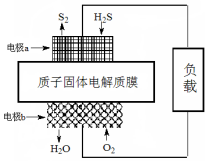 已知:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.下图为H2S燃料电池的示意图.下列说法正确的是( )
已知:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.下图为H2S燃料电池的示意图.下列说法正确的是( )
 已知:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.下图为H2S燃料电池的示意图.下列说法正确的是( )
已知:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.下图为H2S燃料电池的示意图.下列说法正确的是( )| A. | 电极a为电池的负极 | |
| B. | 电极b上发生的电极反应为:O2+2H2O+4e-═4OH- | |
| C. | 电路中每通过4 mol电子,电池内部释放632 kJ热能 | |
| D. | 每34 g H2S参与反应,有2 mol H+经质子膜进入正极区 |
2.下列除去有关物质中杂质(括号内的物质为杂质)的方案中,正确的是( )
| 选项 | 物质 | 除去杂质使用的试剂 | 除去杂质的方法 |
| A | CO2气体(HC1气) | 饱和Na2CO3溶液,浓硫酸 | 洗气 |
| B | NH4Cl固体(I2) | 加热 | |
| C | FeCl2溶液(FeCl3) | 氯水 | |
| D | MgCl2溶液(A1C13) | NaOH溶液,稀盐酸 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
19.已知反应M(g)+3N(g)?2Z(g)△H<0,在密闭容器中反应达到平衡时,N物质的量浓度为0.6mol/L.下列说法正确的是( )
| A. | N的正反应速率是M的逆反应速率的3倍 | |
| B. | 恒温恒容下,通入稀有气体使压强增大,平衡将正向移动 | |
| C. | 恒温下,扩大容器体积至原来的两倍,则N物质的量浓度大于0.6 mol/L | |
| D. | 恒温恒压下,增加Z的物质的量,重新达平衡时,N物质的量浓度大于0.6 mol/L |
6.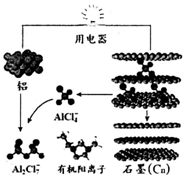 2015年中美专家研制出可在一分钟内完成充电的超常性能铝离子电池,该电池以金属铝和石墨为电极,用AlCl4-、A12C17-和有机阳离子组成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
2015年中美专家研制出可在一分钟内完成充电的超常性能铝离子电池,该电池以金属铝和石墨为电极,用AlCl4-、A12C17-和有机阳离子组成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
 2015年中美专家研制出可在一分钟内完成充电的超常性能铝离子电池,该电池以金属铝和石墨为电极,用AlCl4-、A12C17-和有机阳离子组成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
2015年中美专家研制出可在一分钟内完成充电的超常性能铝离子电池,该电池以金属铝和石墨为电极,用AlCl4-、A12C17-和有机阳离子组成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )| A. | 放电时,电子山石墨电极经用电器流向铝电极 | |
| B. | 充电时,铝电极上发生氧化反应 | |
| C. | 充电时,AlCI4-向铝电极方向移动 | |
| D. | 放电时,负极反应为:Al-3e-+7 AlCl4-═4A12C17- |
16.下列化学反应,能用离子方程式H++OH-=H2O表示的是( )
| A. | 稀硫酸和氢氧化钡溶液 | B. | 稀硫酸和氢氧化钠溶液 | ||
| C. | 盐酸和氢氧化铁 | D. | 碳酸和氨水混合 |
3.下列离子方程式书写正确的是( )
| A. | 钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ | |
| B. | 铁粉溶于浓盐酸:Fe+2H+=Fe2++H2↑ | |
| C. | 铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag | |
| D. | 小苏打溶液中加入盐酸:CO32-+2H+=CO2↑+H2O |
16.下列事实一定能说明HF是弱酸的是( )
| A. | 用HF溶液做导电性实验,灯泡很暗 | |
| B. | HF与水能以任意比混溶 | |
| C. | 1mol/L的HF水溶液能使紫色石蕊试液变红 | |
| D. | 常温下NaF溶液的pH大于7 |