题目内容
16. A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应.
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应.(1)A的名称乙醇;C的分子式为C2H4O2.
(2)写出下列反应的化学方程式:
反应③CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
反应④2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
分析 A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,能与红热的铜丝反应得到D,能与Na反应,能与乙酸反应,A含有羟基,故A为CH3CH2OH,则C为CH3COOCH2CH3,D为CH3CHO,CH3CH2OH燃烧生成二氧化碳与水,CH3CH2OH与Na反应生成CH3CH2ONa与氢气,以此解答该题.
解答 解:(1)由以上分析可知A为乙醇,C为乙酸乙酯,分子式为C2H4O2,故答案为:乙醇;C2H4O2;
(2)反应③为乙醇的酯化反应,方程式为CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,
反应④是乙醇催化氧化生成乙醛,反应方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
点评 本题考查有机物的推断,为高频考点,侧重于学生的分析能力的考查,明确乙醇的性质是解答本题的关键,注意图中反应条件及物质的性质的关系即可解答,题目较简单.

练习册系列答案
相关题目
3.检验SO2中是否有CO2,应采取的方法是( )
| A. | 通过酸性KMnO4后再通过澄清石灰水 | |
| B. | 通过Ba(OH)2溶液再通过石灰水 | |
| C. | 直接通过澄清石灰水 | |
| D. | 通过小苏打悬浊液再通过石灰水 |
4.在粗制CuSO4•5H2O晶体中常含有杂质Fe2+.在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是 ( )
| A. | KMnO4 | B. | H2O2 | C. | Cl2 水 | D. | HNO3 |
11.某温度下,浓度都是1mol•L-1的两种气体X2和Y2,在密闭容器中发生反应生成气体Z,反应2min后,测得参加反应的X2的浓度为0.6mol•L-1,用Y2的浓度变化表示的化学反应速率v(Y2)=0.1mol•L-1•min-1,生成的c(Z)为0.4mol/L.则该反应的化学方程式是( )
| A. | X2+2Y2?2Z | B. | 2X2+Y2?2Z | C. | 3X2+Y2?2Z | D. | X2+3Y2?2Z |
1.甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们在一定条件下的转化关系如图所示(部分产物已略去),下列各组物质中符合图示关系转化的是( )
| 选项 | 物质转化关系 | 甲 | 乙 | 丙 | 丁 |
| A |  | AgNO3(aq) | AgOH(s) | Ag(NH3)2OH(aq) | NH3?H2O(aq) |
| B | S(s) | SO3(g) | SO2(g) | O2(g) | |
| C | NaOH(aq) | NaHCO3(aq) | Na2CO3(aq) | CO2(g) | |
| D | Fe(s) | Fe(NO3)2(aq) | Fe(NO3)3(aq) | HNO3(aq) |
| A. | A | B. | B | C. | C | D. | D |
8.一定质量的铝铁合金溶于足量的NaOH溶液中,完全反应后产生3.36L气体(标准状况下);用同样质量的铝铁合金完全溶于足量的盐酸中,完全反应后产生6.72L气体(标准状况下),则该合金中铝、铁的物质的量之比为( )
| A. | 1:1 | B. | 2:3 | C. | 3:2 | D. | 3:5 |
5.下列说法正确的是( )
| A. | 天然气的主要成分是甲烷 | B. | CH3Cl常温下是液体 | ||
| C. | 石油分馏是化学变化 | D. | 钠融法可以测定有机物的结构 |
6.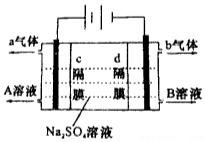 双隔膜电解池的结构示意简图如图所示,利用该装置可以电解硫酸钠溶液以制取硫酸和氢氧化钠,并得到氢气和氧气.对该装置及其原理判断正确的是( )
双隔膜电解池的结构示意简图如图所示,利用该装置可以电解硫酸钠溶液以制取硫酸和氢氧化钠,并得到氢气和氧气.对该装置及其原理判断正确的是( )
 双隔膜电解池的结构示意简图如图所示,利用该装置可以电解硫酸钠溶液以制取硫酸和氢氧化钠,并得到氢气和氧气.对该装置及其原理判断正确的是( )
双隔膜电解池的结构示意简图如图所示,利用该装置可以电解硫酸钠溶液以制取硫酸和氢氧化钠,并得到氢气和氧气.对该装置及其原理判断正确的是( )| A. | a气体为氢气,b气体为氧气 | |
| B. | A溶液为NaOH,B为H2SO4 | |
| C. | c隔膜为阳离子交换膜、d隔膜为阴离子交换膜 | |
| D. | 该电解反应的总方程式可以表示为:2Na2SO4+6H2O$\frac{\underline{\;通电\;}}{\;}$2H2SO4+4NaOH+O2↑+2H2↑ |