题目内容
11.某温度下,浓度都是1mol•L-1的两种气体X2和Y2,在密闭容器中发生反应生成气体Z,反应2min后,测得参加反应的X2的浓度为0.6mol•L-1,用Y2的浓度变化表示的化学反应速率v(Y2)=0.1mol•L-1•min-1,生成的c(Z)为0.4mol/L.则该反应的化学方程式是( )| A. | X2+2Y2?2Z | B. | 2X2+Y2?2Z | C. | 3X2+Y2?2Z | D. | X2+3Y2?2Z |
分析 由信息可知,X2和Y2为反应物,Z为生成物,结合速率之比等于化学计量数之比确定反应方程式,以此来解答.
解答 解:由信息可知,X2和Y2为反应物,Z为生成物,X2、Y2、Z的反应速率之比为$\frac{0.6mol/L}{2min}$:(0.1mol•L-1•min-1):$\frac{0.4mol/L}{2}$=3:1:2,由速率之比等于化学计量数之比可知,反应为3X2+Y2?2Z,
故选C.
点评 本题考查反应速率与化学计量数,为高频考点,把握速率的计算、化学计量数的确定方法为解答本题的关键,侧重分析与计算能力的考查,注意速率与化学计量数的关系,题目难度不大.

练习册系列答案
相关题目
17.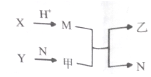 短周期元素A、B、C、D的原子序数依次增加.X、Y、M、N分别由这四种元素中的两种组成的常见化合物,甲、乙为其中两元素对应的单质.若X与Y、甲与乙摩尔质量相同,Y与乙均为淡黄色固体,上述物质之间的转化关系如图所示(部分反应物或生成物省略),则下列说法中正确的是( )
短周期元素A、B、C、D的原子序数依次增加.X、Y、M、N分别由这四种元素中的两种组成的常见化合物,甲、乙为其中两元素对应的单质.若X与Y、甲与乙摩尔质量相同,Y与乙均为淡黄色固体,上述物质之间的转化关系如图所示(部分反应物或生成物省略),则下列说法中正确的是( )
 短周期元素A、B、C、D的原子序数依次增加.X、Y、M、N分别由这四种元素中的两种组成的常见化合物,甲、乙为其中两元素对应的单质.若X与Y、甲与乙摩尔质量相同,Y与乙均为淡黄色固体,上述物质之间的转化关系如图所示(部分反应物或生成物省略),则下列说法中正确的是( )
短周期元素A、B、C、D的原子序数依次增加.X、Y、M、N分别由这四种元素中的两种组成的常见化合物,甲、乙为其中两元素对应的单质.若X与Y、甲与乙摩尔质量相同,Y与乙均为淡黄色固体,上述物质之间的转化关系如图所示(部分反应物或生成物省略),则下列说法中正确的是( )| A. | 相对分子质量M>N,沸点N>M | |
| B. | 常温常压下B的氢化物为气体,C的氢化物为固体 | |
| C. | 原子半径:D>B>C>A | |
| D. | D的最高价氧化物的水合物为强碱 |
18.在空气中不易变质的是( )
| A. | Na2SO3 | B. | 漂白粉 | C. | NaHSO4 | D. | KI溶液 |
6.一定量的CuS和 Cu2S的混合物投入足量的硝酸中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量的NaOH溶液,产生蓝色沉淀,过滤,洗涤,灼烧,得到24.0gCuO.若上述气体为NO和NO2的混合物,且体积比为1:1,则V可能为( )
| A. | 18.0 L | B. | 27.0 L | C. | 31.4 L | D. | 33.6 L |
20.原子通过得电子或失电子形成与Ar原子相同电子层结构的是( )
| A. | Li | B. | Na | C. | O | D. | Cl |
 中学化学中几种常见物质的转化关系如图所示,其中E常温下为无色无味的液体,G为常见的无色气体.
中学化学中几种常见物质的转化关系如图所示,其中E常温下为无色无味的液体,G为常见的无色气体. A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应.
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应.


