题目内容
下列实验过程中,始终无明显现象的是( )
| A、CO2通入CaCl2溶液中 |
| B、NO2通入FeSO4溶液中 |
| C、NH3通入AlCl3溶液中 |
| D、SO2通入已酸化的Ba(NO3)2溶液中 |
考点:二氧化硫的化学性质,氨的化学性质
专题:氧族元素,氮族元素
分析:根据物质之间的反应,如生产气体、沉淀或颜色明显变化,则有明显现象;而反应中生成水或不反应等,则无明显现象,以此来解答.
A、二氧化碳和氯化钙溶液不反应;
B、二氧化氮和水反应生成硝酸具有氧化性氧化亚铁离子;
C、一水合氨和氯化铝反应生成氢氧化铝白色沉淀;
D、二氧化硫溶于水生成亚硫酸,在酸性溶液中,硝酸根离子具有强氧化性
A、二氧化碳和氯化钙溶液不反应;
B、二氧化氮和水反应生成硝酸具有氧化性氧化亚铁离子;
C、一水合氨和氯化铝反应生成氢氧化铝白色沉淀;
D、二氧化硫溶于水生成亚硫酸,在酸性溶液中,硝酸根离子具有强氧化性
解答:
解:A.CO2通入饱和氯化钙溶液中不反应,无明显现象,故A选;
B.NO2通入FeSO4溶液中,二氧化氮和水反应生成硝酸,氧化亚铁离子溶液颜色发生改变,现象明显,故B不选;
C.NH3通入AlCl3溶液中生成氢氧化铝沉淀,有白色沉淀生成,则现象明显,故C不选;
D.SO2通入Ba(NO3)2溶液中,二氧化硫溶于水生成亚硫酸,与硝酸根形成稀硝酸具有氧化性氧化二氧化硫为硫酸,硫酸和钡离子结合生成硫酸钡沉淀,有明显现象,故D不选;
故选A.
B.NO2通入FeSO4溶液中,二氧化氮和水反应生成硝酸,氧化亚铁离子溶液颜色发生改变,现象明显,故B不选;
C.NH3通入AlCl3溶液中生成氢氧化铝沉淀,有白色沉淀生成,则现象明显,故C不选;
D.SO2通入Ba(NO3)2溶液中,二氧化硫溶于水生成亚硫酸,与硝酸根形成稀硝酸具有氧化性氧化二氧化硫为硫酸,硫酸和钡离子结合生成硫酸钡沉淀,有明显现象,故D不选;
故选A.
点评:本题考查物质反应的现象,明确物质的性质及发生的化学反应是解答本题的关键,难度不大.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
 国庆期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,下列关于该物质的说法正确的是( )
国庆期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,下列关于该物质的说法正确的是( )| A、其分子式为C15H18O4 |
| B、分子中只含有1个手性碳原子 |
| C、既能发生加聚反应,又能发生缩聚反应 |
| D、既能与FeCl3溶液发生显色反应,又能使酸性KMnO4溶液褪色 |
下列有关说法正确的是( )
| A、反应SiO2(s)+3C(s)=SiC(s)+2CO(g)室温下不能自发进行,则该反应的△H<0 |
| B、配制硫酸亚铁溶液时,需将FeSO4?7H2O先溶于硝酸再用蒸馏水稀释,最后加少量铁粉 |
| C、0.1 mol?L-1Na2CO3溶液加蒸馏水稀释,CO32-的水解程度增大,溶液的pH减小 |
| D、在硫酸钡悬浊液中加入足量饱和Na2CO3溶液处理,向所得沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3) |
将如图中所示实验装置的K闭合,下列判断正确的是( )


| A、电子沿Zn→a→b→Cu路径流动 |
| B、Cu电极质量增加 |
| C、甲池与乙池中的溶液互换,闭合K,电流没有明显变化 |
| D、片刻后可观察到滤纸b点变红色 |
对于常温下pH为2的盐酸,下列叙述正确的是( )
| A、c(H+)=c(Cl-)+c(OH-)+c(HCl) |
| B、与等体积pH=12的氨水混合后所得溶液显酸性 |
| C、由H2O电离出的c(H+)=1.0×10-12mol?L-1 |
| D、与等体积0.01mol?L-1乙酸钠溶液混合后所得溶液中:c(Cl-)=c(CH3COO-) |
有如图下4种碳架的烃,则下列判断正确的是( )
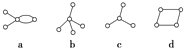

| A、a和d是同分异构体 |
| B、b和c不是同系物 |
| C、a和d都能发生加成反应 |
| D、只有b和c能发生取代反应 |

