题目内容
写出下列化学反应的离子方程式
(1)向H2SO4溶液中逐渐加入Ba(OH)2溶液至中性,写出反应的离子方程式:
(2)碳酸钙放入稀盐酸中的离子方程式为: .
(1)向H2SO4溶液中逐渐加入Ba(OH)2溶液至中性,写出反应的离子方程式:
(2)碳酸钙放入稀盐酸中的离子方程式为:
考点:离子方程式的书写
专题:离子反应专题
分析:(1)硫酸与氢氧化钡等物质的量反应溶液呈中性;
(2)碳酸钙与盐酸反应生成氯化钙、水和二氧化碳.
(2)碳酸钙与盐酸反应生成氯化钙、水和二氧化碳.
解答:
解:(1)硫酸与氢氧化钡等物质的量反应生成硫酸钡和水,离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;
故答案为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;
(2)碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,离子方程式为:CaCO3+2H+=CO2↑+H2O+Ca2+;
故答案为:CaCO3+2H+=CO2↑+H2O+Ca2+.
故答案为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;
(2)碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,离子方程式为:CaCO3+2H+=CO2↑+H2O+Ca2+;
故答案为:CaCO3+2H+=CO2↑+H2O+Ca2+.
点评:本题考查了离子方程式的书写,明确反应的实质和离子方程式书写的方法是解题关键,注意化学式的拆分.

练习册系列答案
相关题目
下列图示与对应的叙述不相符的是( )
A、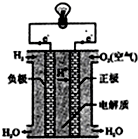 如图表示氢氧燃料电池构造示意图 |
B、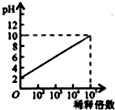 如图表示室温下pH=2的HCl溶液加水稀释倍数与pH的变化关系 |
C、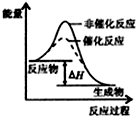 如图表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
D、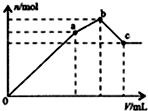 如图表示向NH4 Al(S04)2溶液中逐滴滴人Ba(OH)2溶液,生成沉淀总物质的量(n)随 着Ba(OH)2溶液体积(y)的变化 |
用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4 L H2O的分子数为1NA |
| B、物质的量浓度为0.5 mol?L-1的MgCl2溶液,含有Cl-数为1 NA |
| C、0.1molNa2O2晶体中阴离子数为6.02×1022 |
| D、常温常压下,14 g N2含有分子数为0.5 NA |
下列叙述正确的是( )
| A、1 mol H2O的质量为18g/mol |
| B、CH4的摩尔质量为16g |
| C、阿伏伽德罗常数个SO2分子的质量为64g |
| D、标准状况下,1 mol任何物质体积均为22.4L |
离子方程式H++OH-=H2O能表示的化学反应是( )
| A、Ca(OH)2+2CH3COOH=(CH3COO)2Ca+2H2O |
| B、HCl+NH3?H2O=NH4Cl+H2O |
| C、2HNO3+Ba(OH)2=Ba(NO3)2+2H2O |
| D、Mg(OH)2+H2SO4=MgSO4↓+2H2O |
生活处处有化学,下列说法正确的是( )
| A、氢氧化铝可作胃酸过多的中和剂 |
| B、福尔马林可作食品的保鲜剂 |
| C、用聚乙烯塑料代替聚乳酸塑料可减少白色污染 |
| D、煎炸食物的花生油、牛油都属于可皂化的饱和酯类 |



