题目内容
要除去下列各物质中混有的杂质,请写出其所用试剂的化学式(或方法)及有关反应的化学方程式(或离子方程式):
(1)除去氯化亚铁溶液中混有的少量氯化铜:试剂(或方法) ;离子方程式 .
(2)除去食盐溶液中混有的少量氯化镁:试剂(或方法) ;离子方程式 .
(3)除去碳酸钠粉末中混有的少量碳酸氢钠:试剂(或方法) ;化学方程式 .
(1)除去氯化亚铁溶液中混有的少量氯化铜:试剂(或方法)
(2)除去食盐溶液中混有的少量氯化镁:试剂(或方法)
(3)除去碳酸钠粉末中混有的少量碳酸氢钠:试剂(或方法)
考点:物质的分离、提纯的基本方法选择与应用,物质的分离、提纯和除杂
专题:化学实验基本操作
分析:(1)Fe与氯化铜反应生成氯化亚铁和Cu,然后过滤可除杂;
(2)氯化镁与NaOH反应生成NaCl和沉淀,然后过滤可除杂;
(3)碳酸氢钠受热分解生成碳酸钠.
(2)氯化镁与NaOH反应生成NaCl和沉淀,然后过滤可除杂;
(3)碳酸氢钠受热分解生成碳酸钠.
解答:
解:(1)Fe与氯化铜反应生成氯化亚铁和Cu,然后过滤可除杂,则除杂试剂为Fe粉,离子反应为Fe+Cu2+═Fe2++Cu,故答案为:Fe粉;Fe+Cu2+═Fe2++Cu;
(2)氯化镁与NaOH反应生成NaCl和沉淀,然后过滤可除杂,则除杂试剂为NaOH溶液,离子反应为Mg2++2OH-═Mg(OH)2↓,
故答案为:NaOH溶液;Mg2++2OH-═Mg(OH)2↓;
(3)碳酸氢钠受热分解生成碳酸钠,则除杂方法为加热,化学反应为2NaHCO3
Na2CO3+CO2↑+H2O,故答案为:加热;2NaHCO3
Na2CO3+CO2↑+H2O.
(2)氯化镁与NaOH反应生成NaCl和沉淀,然后过滤可除杂,则除杂试剂为NaOH溶液,离子反应为Mg2++2OH-═Mg(OH)2↓,
故答案为:NaOH溶液;Mg2++2OH-═Mg(OH)2↓;
(3)碳酸氢钠受热分解生成碳酸钠,则除杂方法为加热,化学反应为2NaHCO3
| ||
| ||
点评:本题考查物质的分离、提纯方法及选择,为高频考点,把握物质的性质及除杂的原则为解答的关键,注意发生的化学反应,题目难度不大.

练习册系列答案
相关题目
分析离子反应 xR2++yH++O2═mR3++nH2O,下列说法中正确的是( )
| A、n=2,H2O是氧化产物 |
| B、x=y=m=4 |
| C、该反应中R2+得到电子,被氧化为R3+ |
| D、任何氧化还原反应中氧化剂失电子总数都等于还原剂得电子总数 |
下列图中所示实验操作不合理的是( )
A、 读取液体体积 |
B、 称量NaOH固体 |
C、 熄灭酒精灯 |
D、 检查装置的气密性 |
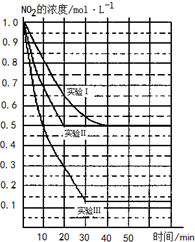 某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g)△H>0.在三种不同条件下进行,其中NO、O2的起始浓度都为1.0mol/L,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol?L-1)随时间(min)的变化如图所示.请回答下列问题:
某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g)△H>0.在三种不同条件下进行,其中NO、O2的起始浓度都为1.0mol/L,实验Ⅰ、Ⅱ反应温度相同,NO2的浓度(mol?L-1)随时间(min)的变化如图所示.请回答下列问题: