题目内容
在一定体积的密闭容器内,发生反应CO2(g)+H2(g)?CO(g)+H2O(g)化学平衡常数K随温度的变化如表:
(1)写出该反应的化学平衡常数表达式:K=
(2)该反应是 热反应.(填吸热或放热)
(3)能说明该反应已经达到平衡状态的是 .(多选题)
a.c (CO2)=c (CO)
b.容器内压强保持不变
c.混合气体中CO2的体积分数不变
d.容器内的密度保持不变
(4)在某温度时,平衡浓度符合下式:[CO].[H2O]=1.7[CO2].[H2],试判断此时的温度为 .
| 温度t(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(2)该反应是
(3)能说明该反应已经达到平衡状态的是
a.c (CO2)=c (CO)
b.容器内压强保持不变
c.混合气体中CO2的体积分数不变
d.容器内的密度保持不变
(4)在某温度时,平衡浓度符合下式:[CO].[H2O]=1.7[CO2].[H2],试判断此时的温度为
考点:化学平衡状态的判断,化学平衡建立的过程
专题:化学平衡专题
分析:(1)根据化学平衡常数的概念以及反应的方程式书写;
(2)根据温度对化学平衡、化学平衡常数的影响判断;
(3)平衡标志一个是正逆反应速率相同,另一个是各组分的含量保持不变,依据反应是气体体积不变的吸热反应结合选项分析判断是否正确;
(4)根据浓度和平衡常数来计算平衡常数,从而确定温度.
(2)根据温度对化学平衡、化学平衡常数的影响判断;
(3)平衡标志一个是正逆反应速率相同,另一个是各组分的含量保持不变,依据反应是气体体积不变的吸热反应结合选项分析判断是否正确;
(4)根据浓度和平衡常数来计算平衡常数,从而确定温度.
解答:
解:(1)因平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,所以K=
,
故答案为:
;
(2)化学平衡常数的大小只与温度有关,升高温度,平衡向吸热的方向移动,由表可知:升高温度,化学平衡常数增大,说明化学平衡正向移动,因此正反应方向吸热,故答案为:吸热;
(3)a.当反应达到平衡状态是各物质的浓度保持不变,但是浓度不一定相等,所以c (CO2)=c (CO),不能说明达到平衡状态,故a错误;
b.该反应为气体的物质的量不变的反应,则容器中压强始终不变,不能作为判定平衡的方法,故b错误;
c.当反应达到平衡状态是各物质的浓度保持不变,混气体中各物质的含量保持不变,所以混合气体中CO2的体积分数不变,说明达到平衡状态,故c正确;
d.容器的体积不变,气体的质量守恒,所以容器内的密度始终保持不变,所以不能用密度来判断平衡状态,故d错误;
故答案为:c;
(4)在某温度时,平衡浓度符合下式:[CO].[H2O]=1.7[CO2].[H2],则平衡常数K=1.7,则该温度为1000℃,
故答案为:1000℃.
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
故答案为:
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
(2)化学平衡常数的大小只与温度有关,升高温度,平衡向吸热的方向移动,由表可知:升高温度,化学平衡常数增大,说明化学平衡正向移动,因此正反应方向吸热,故答案为:吸热;
(3)a.当反应达到平衡状态是各物质的浓度保持不变,但是浓度不一定相等,所以c (CO2)=c (CO),不能说明达到平衡状态,故a错误;
b.该反应为气体的物质的量不变的反应,则容器中压强始终不变,不能作为判定平衡的方法,故b错误;
c.当反应达到平衡状态是各物质的浓度保持不变,混气体中各物质的含量保持不变,所以混合气体中CO2的体积分数不变,说明达到平衡状态,故c正确;
d.容器的体积不变,气体的质量守恒,所以容器内的密度始终保持不变,所以不能用密度来判断平衡状态,故d错误;
故答案为:c;
(4)在某温度时,平衡浓度符合下式:[CO].[H2O]=1.7[CO2].[H2],则平衡常数K=1.7,则该温度为1000℃,
故答案为:1000℃.
点评:本题考查化学平衡的计算,明确平衡常数的计算方法及平衡常数与反应方程式的关系、平衡的判定等即可解答,题目难度中等.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列说法不正确的是( )
| A、N2和H2在一定条件下合成氨,可以实现固氮 |
| B、用氨水吸收CO2,可以捕捉碳,降低温室效应 |
| C、对煤炭、石油脱硫,可以减少酸雨 |
| D、PM2.5是指大气中直径接近2.5微米的颗粒物,入肺影响健康.它在空气中为气溶胶 |
设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、常温常压下,NA个CO2分子的体积为22.4L |
| B、常温常压下,1mol氦气含有的核外电子数为4 NA |
| C、12.4g白磷(P4)中含有的磷原子数为0.4 NA |
| D、标准状况下,22.4L氧气所含质子数是8NA |
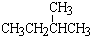 ; ⑧CH3CH2CH2CH3与CH3CH(CH3)2
; ⑧CH3CH2CH2CH3与CH3CH(CH3)2